Die Diagnose einer H.-pylori-Infektion wird typischerweise beim Gastroenterologen gestellt, dagegen erfolgt die Behandlung in der Regel in der allgemeinmedizinischen Praxis. Was die Indikation zur Therapie angeht, gibt es auch in Deutschland einen Paradigmenwechsel, welcher sich in der aktuell überarbeiteten deutschen Leitlinie wiederfinden wird. Aufgrund der Zunahme von Antibiotikaresistenzen ist die Therapie schwieriger geworden, deshalb soll hier das aktuelle therapeutische Vorgehen vorgestellt werden.
Helicobacter pylori ist die Ursache der chronischen Typ-B-Gastritis, welche bei etwa 20 % der Infizierten zu Komplikationen wie Dyspepsie, peptisches Ulkus, Magenkarzinom und MALT-Lymphom führt [1]. In Deutschland ist aktuell noch etwas mehr als ein Viertel der Bevölkerung mit H. pylori infiziert, wobei Unterschiede in Abhängigkeit von der regionalen und ethnischen Herkunft bestehen [2]. Die Infektion mit H. pylori erfolgt typischerweise in der frühen Kindheit. Es zeigt sich eine kontinuierliche Abnahme der Prävalenz bei den Kindern und Jugendlichen, welche aktuell unter 10 % in Deutschland liegt [3].
Paradigmenwechsel: H. pylori eine Infektionskrankheit
Basierend auf dem Befund, dass die H.-pylori-Gastritis immer strukturelle und funktionelle Veränderungen verursacht, wurde bereits beim internationalen Kyoto-Konsensus-Treffen die H.-pylori-Infektion als Infektionskrankheit definiert, und zwar unabhängig vom Vorliegen von Symptomen oder Komplikationen [4]. Dieser Paradigmenwechsel hat nun auch Eingang in die überarbeitete deutsche H.-pylori-Leitlinie gefunden, welche bereits konsentiert, aber noch nicht publiziert ist. Daraus folgt, dass der Nachweis einer H.-pylori-Gastritis prinzipiell eine Indikation für eine Therapie darstellt. Im klinischen Alltag ergibt sich somit die Frage, bei welchen Symptomen oder Erkrankungen gezielt nach H. pylori gefahndet werden soll.
- peptisches Ulkus
- MALT-Lymphom
- Dyspepsie/Reizmagen
- ASS/NSAR Blutung/Prophylaxe
- Magenkarzinomprophylaxe bei Risikopersonen
- Eisenmangelanämie
- ITP
Wann nach H. pylori suchen?
Bei jeder H.-pylori-Diagnostik sollte berücksichtigt werden, dass Protonenpumpenhemmer bereits zwei Wochen und jede antibiotische Therapie vier Wochen vor der geplanten Diagnostik abgesetzt werden sollten, weil diese Medikamente zu falsch negativen Ergebnissen führen können. Kasten 1 fasst die Erkrankungen zusammen, bei denen eine H.-pylori-Diagnostik erfolgen soll. In der Ätiologie des peptischen Ulkus ist H. pylori beim Ulcus duodeni zahlenmäßig noch führend, während beim Magenulkus Medikamente, insbesondere nichtsteroidale Antirheumatika (NSAR), häufiger gefunden werden. Bei Vorliegen eines H.-pylori-Ulkus führt eine Eradikation zu einem weitgehenden Rückgang der Rezidive und von Ulkuskomplikationen. Beim seltenen MALT-Lymphom kann stadienabhängig alleine durch die Keim-
eradikation eine Remission in 75 % der Fälle erreicht werden. Bei H. pylori-positivem Reizmagen kann durch eine erfolgreiche Therapie in bis zu 10 % eine Symptomfreiheit erzielt werden. Ebenso soll H. pylori bei Patient:innen, die unter NSAR oder niedrigdosiertem ASS bluten oder die eine Ulkusanamnese aufweisen, untersucht werden. Weitere Indikationen sind die Magenkrebsprophylaxe bei Risikopersonen, die Eisenmangelanämie nach vorheriger vollständiger endoskopischer Abklärung und die idiopathische thrombozytopenische Purpura (ITP).
Wovon hängt der Erfolg einer H.-pylori-Therapie ab?
Der wichtigste Faktor für eine erfolgreiche H.-pylori-Therapie ist die richtige Wahl von Antibiotika mit Empfindlichkeit gegenüber dem Keim. Lange Zeit war die Clarithromycin-basierte Tripeltherapie der weltweite Therapiestandard. Aufgrund einer wachsenden Clarithromycinresistenz verliert diese Therapie aber zunehmend ihre Wirksamkeit. Für Deutschland beträgt die primäre Resistenz für Clarithromycin global 15 %, allerdings bestehen große individuelle und regionale Unterschiede [2]. Eine Makrolidvortherapie führt häufig zu einem Wirkverlust von Clarithromycin. Bisher wurde in der deutschen Leitlinie vor Therapieeinleitung eine individuelle Risikoabschätzung bezüglich einer Antibiotikaresistenz gefordert. Dieses Vorgehen hat sich im klinischen Alltag nicht bewährt und wird daher in der überarbeiteten Leitlinie nicht mehr empfohlen. Weitere Einflussfaktoren des Therapieerfolges sind die Therapiedauer (zweiwöchige Therapieregimes erhöhen Eradikationsraten um ca. 10 % gegenüber den einwöchigen), Begleiterkrankungen (bei Diabetes niedrigere Eradikationsraten), das Ausmaß der Säurehemmung und Verzicht auf Rauchen.
Wie behandle ich die H.-pylori-Infektion?
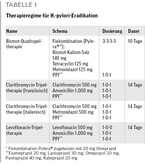
Bei nachgewiesener H.-pylori-Infektion ist die Bismut-Quadrupeltherapie der neue Standard in der Erstlinientherapie (Abb. 1). Aufgrund der schwieriger gewordenen Therapie empfiehlt die überarbeitete deutsche Leitlinie bereits nach erfolgloser Erstlinientherapie eine Resistenztestung mit anschließender testgerechter Zweitlinientherapie. Als Optionen stehen hier eine zweiwöchige Levofloxacin-Tripeltherapie oder eine Clarithromycin-Tripeltherapie zur Verfügung. Bei erneutem Therapieversagen sollte dann eine Vorstellung in einer spezialisierten gastroenterologischen Praxis erfolgen.
Welche Nachkontrollen sind notwendig?
Der Erfolg einer H.-pylori-Therapie soll immer überprüft werden. Diese Nachkontrolle soll frühestens vier Wochen nach Ende der Antibiotikatherapie erfolgen. Auch eine PPI-Behandlung soll mindestens zwei Wochen vor Testung abgesetzt werden. Wenn aus klinischen Gründen keine Endoskopie-Indikation besteht, können nichtinvasive Testverfahren wie der 13C-Atemtest oder ein Stuhlantigentest für die Erfolgskontrolle verwendet werden.
- Paradigmenwechsel bei der Therapie: Allein der Nachweis von H. pylori genügt als Therapieindikation.
- Die Bismut-Quadrupeltherapie ist neuer Erstlinien-Standard.
- Nach Versagen der Erstlinientherapie sollte eine Resistenztestung erfolgen.
- Vier Wochen nach Ende der Antibiotikatherapie sollte immer eine Erfolgskontrolle erfolgen.
Erschienen in: doctors|today, 2022; 2 (2) Seite 32-34