Neueste Studiendaten zur Pathogenese und Therapie von androgenetischer Alopezie (AGA), frontal fibrosierender Alopezie (FFA) und Alopecia areata (AA) präsentierte Prof. Dr. Ulrike Blume-Peytavi, Charité Berlin, bei einem Plenarvortrag auf der FOBI in München.
Finasterid war für die Behandlung bei androgenetischer Alopezie (AGA) bislang ausschließlich in Tablettenform verfügbar – oder als individuelle topische Zubereitung. Nun wurde auch ein standardisiertes topisches Arzneimittel mit Finasterid (Fynzur® Spray; 2,275 mg/ml, 1 – 4 Sprühstöße à 50 µg) in einer randomisiert-kontrollierten Studie (RCT) erfolgreich untersucht, berichtete Prof. Dr. Ulrike Blume-Peytavi, Berlin.
Topisches Finasterid für männliche AGA-Patienten
In der kürzlich publizierten Studie, an der Blume-Peytavi maßgeblich beteiligt war, wurde die systemische Anwendung (oral, 1 mg/d) vs. topische Anwendung von Finasterid verglichen. Die Lokaltherapie wurde mithilfe eines Sprüh-Applikators auf die betroffenen Areale der Kopfhaut aufgetragen. In einem dritten Studienarm lief Placebo [1].
„Unter der topischen Anwendung waren die Finasteridspiegel im Plasma um den Faktor 100 niedriger als bei der oralen Therapie“, berichtete die Expertin den Vorteil der topischen Anwendung. Die Konzentration an Dihydrotestosteron (DHT) sank aber unter dem Topikum weniger stark ab als unter der Systemtherapie (-34,5 % vs. -55,6 %). Die Zunahme der Haardichte war unter der topischen vs. oralen Finasteridgabe vergleichbar: Nach 12 Wochen wurden durchschnittlich +20,4 vs. +22,5 Haare/cm² gezählt. Nach 24 Wochen waren es +20,2 vs. +21,1 Haare/cm²; dies war der primäre Wirksamkeitsendpunkt. Der Zuwachs an Haardichte war in beiden aktiven Studienarmen jeweils signifikant größer als im Placeboarm (p < 0,001) [1].
Im Juni 2022 hat die topische Finasteridtherapie die europäische Zulassung erhalten. Diese gilt für männliche Patienten mit AGA im Stadium III bis V (Vertex). Das pharmakologisch geprüfte und zugelassene Arzneimittel soll voraussichtlich ab Ende des Jahres 2022 verfügbar sein. „Die neue Formulierung von Finasterid ermöglicht bei Männern eine signifikante Verbesserung der Haardichte unter lokaler Anwendung trotz niedrigerer Finasterid-Serumspiegel als bei oraler Gabe und gutem Sicherheitsprofil“, fasste Blume-Peytavi zusammen.
Minoxidil als Tablette bei AGA?
Gerade umgekehrt ist die Fragestellung bei Minoxidil: Kann der Wirkstoff, der bislang topisch aufgetragen wird, auch bequem als Tablette eingenommen werden, fragen sich laut Blume-Peytavi etliche Patienten. Dieses Vorgehen sei international (off-label!) sehr populär, berichtete sie. So wird systemisches Minoxidil etwa in Spanien oder Australien in niedriger Dosis (0,5 – 1 mg/d bei Frauen und 2,5 – 5 mg/d bei Männern) in dieser Indikation eingesetzt. Es fehlen jedoch randomisierte placebokontrollierte Studien hierzu.
Minoxidil wird bekanntlich auch zur Blutdrucksenkung angewendet, jedoch „wegen seiner Nebenwirkungen nur als Reserve-Antihypertensivum“, erinnerte Blume-Peytavi. „Selbst unter der niedrig dosierten oralen Gabe kam es als häufigste Nebenwirkung in etwa 15 % zu einer Hypertrichose“, gab sie zu bedenken. Ein solches unkontrolliertes Haarwachstum am Körper könne auch schon unter den niedrigsten Dosen auftreten [2, 3]. „Eine Anwendung von Minoxidil-Tabletten bei androgenetischer Alopezie erfolgt nach wie vor off-label und unterliegt der Verantwortung des Arztes“, so die Dermatologin.
Frontal fibrosierende Alopezie (FFA): Pathomechanismus noch nicht vollständig geklärt
„Vernarbende Alopezien (Abb. 1) betreffen zwar nur eine kleine Patientengruppe, sie sind jedoch irreversibel“, betonte Blume-Peytavi. Deshalb sollten sie intensiver als bislang erforscht werden. Einige neue Daten gibt es zum Pathomechanismus: „Ursache ist ein Kollaps des Immunprivilegs, der letztlich zu einer Zerstörung der Stammzellen in der Wulstregion führt“, so Blume-Peytavi. Bei der Erkrankung scheine eine genetische Prädisposition eine Rolle zu spielen. Ob auch hormonelle Einflüsse bei der FFA von Bedeutung sind, sei noch nicht abschließend geklärt [4].
Fortschritte gibt es indes bei der Diagnosestellung: Die Kriterien wurden international einheitlich definiert. Blume-Peytavi verwies hierzu auf eine eigene Arbeit sowie auf die aktuellen Leitlinien [4, 5].
Für die symptomatische Therapie der FFA werden in der entzündlichen Phase der Erkrankung topische Steroide (etwa Clobetasolpropionat oder Betamethasonvalerat topisch-okklusiv, oder Triamcinolonacetat intraläsional eingesetzt, konstatierte die Dermatologin. Später sei u. a. eine (Off-Label-)Anwendung von Tacrolimus oder Pimecrolimus in der Übergangszone am Haaransatz möglich. Tritt innerhalb von sechs Monaten kein Erfolg ein, ist eine systemische Zweitlinientherapie mit niedrig dosiertem (50 mg) Doxycyclin oder z. B. mit Hydroxychloroquin (5 mg/kg) angezeigt [4].
AA: JAK-Inhibitoren bringen den Durchbruch
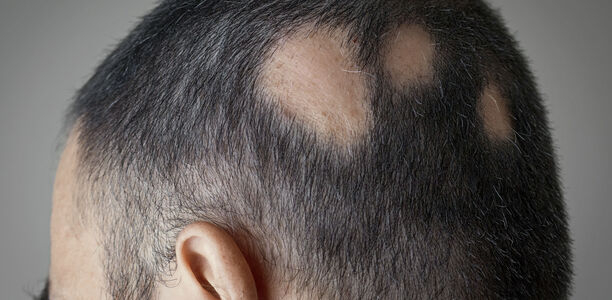
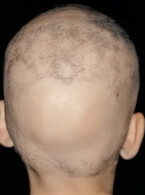
Bei der AA (Abb. 2) greifen zytotoxische T-Zellen den Haarbulbus an und durchbrechen das Immunprivileg. Die Proliferation der Matrix-Keratinozyten wird unterbrochen, weitere Immunzellen werden aktiviert und entzündliche Signalwege werden angestoßen. „Wenn wir dann den JAK-STAT-Signalweg nicht unterbrechen, setzt ein Circulus vitiosus ein, die Feedback-Schleife verstärkt sich immer weiter“, beschrieb Blume-Peytavi neueste Erkenntnisse zum Pathomechanismus der AA [6].
Zufällige Beobachtungen zeigten einen günstigen Einfluss der JAK-Inhibitoren auf das Nachwachsen des Haars bei AA-Patienten. Derzeit laufen zahlreiche Studien zu dieser Frage; Blume-Peytavi stellte drei Kandidaten für die künftige JAK-Hemmer-Therapie bei AA vor. So zeigte Ruxolitinib in einer Phase-II-Studie bei Patienten mit moderater bis schwerer AA eine deutliche Reduktion des SALT-Scores um ≥ 50 %: Immerhin 58 % der Patienten erreichten mit 2-mal täglich 12 mg Ruxolitinib diesen klinisch bedeutsamen Behandlungserfolg [7].
In einer Phase-IIa-Studie konnte man mit Ritlecitinib und Brepocitinib ebenfalls eine signifikante Verbesserung des SALT-Scores bei moderat bis schwer betroffenen AA-Patienten erzielen [8].
Baricitinib vor Kurzem für Alopecia areata (AA)-Patienten zugelassen
Baricitinib wurde bereits in zwei Phase-III-Studien untersucht. Einen SALT-Score (Schweregrad der AA) von (absolut) ≤ 20 erreichten mit der 4-mg-Dosis in 36 Wochen 38,8 % der Patienten (BRAVE-AA1-Studie) bzw. 35,9 % der Patienten (BRAVE-AA2-Studie) [9].
„Damit können wir nun erstmals eine Autoimmunerkrankung des Haars zielgerichtet therapieren. Das ist ein Durchbruch“, freute sich Blume-Peytavi. Die besten Erfolgsaussichten für die Behandlung mit einem JAK-Inhibitor bestehen nach ihren Worten bei Patienten mit schwerer AA, also mit einem SALT-Score von 50 bis 95. Bei einer sehr schweren AA (totalis/universalis) dagegen seien die Erfolgschancen nur etwa halb so groß, wie eine Posterpräsentation beim AAD-Kongress zur Behandlung mit Baricitinib gezeigt habe.
„Die EMA hat die Behandlung mit Baricitinib 4 mg für die schwere AA (SALT-Score > 50) am 20. Juni 2022 zugelassen“, sagte die Dermatologin. Somit steht Baricitinib als erster JAK-Inhibitor für die Indikation schwere AA zur Verfügung. Eine automatische Erstattung der Verordnungskosten für Arzneimittel gegen Haarverlust ist leider bislang durch das Gesetz ausgeschlossen.
Erschienen in: DERMAforum, 2022; 26 (12) Seite 4