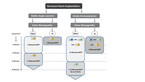
Die duale antithrombozytäre Therapie (DAPT) mit ASS und einem P2Y12-Inhibitor ist nach einer koronaren Stent-Implantation unerlässlich. Das Ziel dieser medikamentösen Nachbehandlung: die Verhinderung von Stentthrombosen und die Prävention von kardiovaskulärem Tod und Herzinfarkt durch eine Progression der koronaren Grunderkrankung. Die Art und Dauer der DAPT-Therapie erfolgt heute immer individueller und richtet sich nach dem Ischämie- und Blutungsrisiko.
Die DAPT ist seit 23 Jahren wesentlicher Bestandteil der Medikation nach koronarer Stent-Implantation [1]. Durch die Fortentwicklung der (beschichteten) Drug-eluting Stents spielen (unbeschichtete) Bare-metal Stents heute bei der Koronarintervention keine Rolle mehr: Die DAPT richtet sich nicht mehr nach dem Stenttyp, sondern individualisiert nach klinischem Erscheinungsbild sowie Ischämie- und Blutungsrisiko [2].
DAPT bei stabiler Angina pectoris
Die DAPT nach koronarer Stent-Implantation bei stabiler Angina pectoris besteht aus ASS und dem P2Y12-Inhibitor Clopidogrel. In der Regel wird eine DAPT von sechs Monaten empfohlen (nach Metaanalysen). Abhängig von Ischämie- und Blutungsrisiko kann man im Einzelfall nach kritischer Risiko-Nutzen-Abwägung davon abweichen. Risiko-Scores helfen hier bei der Entscheidungsfindung (vgl. Abb. 1).
Bei erhöhtem Blutungsrisiko (PRECISE-DAPT-Score ≥ 25) kann der Arzt die DAPT auf drei Monate verkürzen [3, 4] und eine weitere Kürzung (bei extrem hohem Blutungsrisiko, operativen Eingriffen) erwägen, darf dabei aber eine Mindestdauer von einem Monat nicht unterschreiten [5].
Für eine Verlängerung der antithrombozytären Therapie auf bis zu 30 Monate sollte man sich nur bei deutlich erhöhtem Ischämierisiko (DAPT-Score ≥ 2) und nach sorgfältiger Risiko-Nutzen-Abwägung entscheiden, da in der DAPT-Studie die Blutungskomplikationen stark erhöht waren (Abb. 2) [6, 7].
Jede Verkürzung oder Verlängerung der DAPT sollte der Arzt mit dem kardiologischen Zentrum der Stent-Implantation besprechen.
DAPT bei akutem Koronarsyndrom
Bei akutem Koronarsyndrom besteht langfristig ein deutlich höheres ischämisches Risiko als bei stabiler Angina pectoris. Hier sollte man als P2Y12-Inhibitor Prasugrel oder Ticagrelor verordnen [8, 9]. Clopidogrel kommt nur in Betracht, wenn die beiden potenteren P2Y12-Inhibitoren kontraindiziert sind, nicht vertragen werden oder bei zusätzlicher Indikation zur oralen Antikoagulation. Die aktuelle ISAR-REACT-5-Studie zeigt deutliche Vorteile von Prasugrel im Vergleich zu Ticagrelor hinsichtlich kardiovaskulärer Ereignisse, sodass man diese Substanz bevorzugen [10], bei der Auswahl des P2Y12-Inhibitors allerdings immer Kontraindikation und Nebenwirkungsprofil berücksichtigen sollte.
Bei akutem Koronarsyndrom sollte man die DAPT für zwölf Monate verordnen [8, 9, 11]. Bei erhöhtem Blutungsrisiko (PRECISE-DAPT-Score ≥ 25) lässt sich die Dauer auf sechs Monate reduzieren [12, 13]. In Abhängigkeit einer Nutzen-Risiko-Abwägung kann auch beim akuten Koronarsyndrom eine längere DAPT über zwölf Monate hinaus sinnvoll sein. Vor allem bei hohem Ischämierisiko und niedrigem Blutungsrisiko kann man nach der PEGASUS-Studie eine DAPT-Verlängerung mit Ticagrelor in reduzierter Dosis (2-mal 60 mg/Tag) bis zu drei Jahre nach Infarkt fortführen (Abb. 2) [14]. Auch hier ist die Rücksprache mit dem primär versorgenden Zentrum zu empfehlen.
DAPT-Deeskalation
Überwiegt beim akuten Koronarsyndrom das Blutungsrisiko, kann eine Deeskalation von einem potenten P2Y12-Inhibitor (Prasugrel oder Ticagrelor) zu Clopidogrel innerhalb der ersten vier Wochen nach Infarkt bedacht werden [15, 16],
da der größte Benefit eines potenten P2Y12-Inhibitors im Vergleich zu Clopidogrel – die Verhinderung kardiovaskulärer Ereignisse in den ersten Tagen nach Infarkt – nachweisbar ist [17]. Sowohl die Deeskalation eines potenten P2Y12-Inhibitors zu Clopidogrel nach einem Monat (TOPIC-Studie) als auch nach einer Woche (TROPICAL-ACS-Studie) war gegenüber einer zwölfmonatigen Therapie mit einem potenten P2Y12-Inhibitor hinsichtlich kardiovaskulärer Ereignisse nicht unterlegen. Die Deeskalation, gesteuert durch das Ergebnis eines Thrombozytenfunktionstests zur Identifizierung von Clopidogrel-Non-Respondern (TROPICAL-ACS-Studie), könnte zusätzlich nutzen.
Dauertherapie nach DAPT
Nach einer DAPT wird in der Sekundärprophylaxe weiterhin die Dauertherapie mit ASS empfohlen [18]. Bei ASS-Unverträglichkeit kann man alternativ den P2Y12-Inhibitor Clopidogrel verordnen [19]. Die COMPASS-Studie untersuchte eine Intensivierung der sekundärprophylaktischen Therapie bei manifester koronarer Herzerkrankung (KHK) auf ASS plus dem Faktor-X-Inhibitor Rivaroxaban in niedriger Dosis (2-mal 2,5 mg/Tag) [20, 21].
Damit ließ sich bei stabiler KHK das Risiko kardiovaskulärer Ereignisse signifikant senken.
Eine neue Studie zeigt, dass man durch Risikostratifizierung mit dem REACH- oder CART-Score die Patienten mit hohem ischämischem Risiko identifizieren kann, die besonders von der intensivierten Sekundärprophylaxe mit ASS plus Rivaroxaban profitieren [22]. Eine abschließende Empfehlung in den Leitlinien steht dafür aber noch aus.
Antikoagulation
Etwa 6 – 8 % aller Patienten mit koronarer Stent-Implantation haben die Indikation für eine dauerhafte orale Antikoagulation. Die häufigste Indikation ist die Prävention des Schlaganfalls bei Vorhofflimmern. Diese Patienten wurden bislang meist mit einer sogenannten "Triple-Therapie" aus oraler Antikoagulation plus DAPT behandelt. Allerdings führt dies zu einem zwei- bis dreifach erhöhten Blutungsrisiko [23 – 26]. Eine DAPT allein schützt nur unzureichend vor Schlaganfall [27].
Eine alleinige orale Antikoagulation der DAPT ist bei der Prävention kardiovaskulärer Ereignisse nach Stent-Implantation aber unterlegen [1].
In den letzten Jahren untersuchte man für diese Patienten in einigen Studien verschiedene Therapieoptionen, die bei maximalem Schutz vor kardio- und zerebrovaskulär ischämischen Ereignissen das Blutungsrisiko möglichst minimieren sollten [23, 28 – 30]. Auf Basis dieser Daten sollte die Triple-Therapie so kurz wie möglich verordnet werden. Um in dieser Phase das Blutungsrisiko zu minimieren, sollte man präventiv vorgehen, etwa mit Protonenpumpenhemmern, und die orale Antikoagulation nicht mit potenten P2Y12-Inhibitoren (Prasugrel oder Ticagrelor) kombinieren.
Die Dauer der Triple-Therapie hängt von einer gründlichen Abklärung des Ischämie- und Blutungsrisikos ab. Bei vorwiegendem Ischämierisiko (z. B. bei akutem Koronarsyndrom oder nach komplexen Interventionen) sollte diese einen Monat dauern und sich ansonsten auf die periprozedurale Zeit des Krankenhausaufenthalts beschränken. Danach sollte man die orale Antikoagulation mit einem einzelnen Plättchenhemmer bis zwölf Monate nach der Stent-Implantation fortführen, bei hohem Blutungsrisiko die antithrombozytäre Therapie schon nach sechs Monaten absetzen (Abb. 3). Das Blutungsrisiko lässt sich mit dem HAS-BLED-Score abschätzen.
Während der Triple-Therapie ist es ratsam, die Dosis der oralen Antikoagulation anzupassen. In Kombination mit Vitamin-K-Antagonisten sollte der INR-Wert am unteren Ende des empfohlenen therapeutischen Bereichs liegen (INR 2,0 – 2,5 bei Vorhofflimmern). Bei der Verwendung der neuen oralen Antikoagulanzien (NOAK) sollte der Patient während der Triple-Therapie die niedrigere zur Schlaganfallprophylaxe zugelassene Dosis erhalten. In Kombination mit einem einzelnen Plättchenhemmer kann sowohl bei der Verwendung von Vitamin-K-Antagonisten als auch bei NOAK die übliche zur Schlaganfallprophylaxe empfohlene Dosis verordnet werden. Eine Ausnahme ist dabei Rivaroxaban, das laut PIONEER-AF-PCI-Studie kombiniert mit einem einzelnen Plättchenhemmer auch eine niedrige Dosis möglich macht (1-mal 15 mg/Tag) (Abb. 3).
Dauertherapie bei Indikation zur Antikoagulation
Bei einer Indikation zur dauerhaften oralen Antikoagulation kann man die antithrombozytäre Therapie in der Regel nach zwölf Monaten vollständig absetzen. Eine zusätzliche Gabe von ASS über ein Jahr hinaus ergab in den Studien keinen zusätzlichen Nutzen, so dass hier eine Monotherapie mit oraler Antikoagulation ausreicht [31]. Die kürzlich publizierte AFIRE-Studie bestätigt das Konzept der alleinigen Antikoagulation [32].
Eine dauerhafte intensivierte Therapie von oraler Antikoagulation mit ASS oder Clopidogrel sollte nur bei Patienten mit deutlich erhöhtem Ischämierisiko und mechanischer Klappenprothese erwogen werden.
Fazit für die Praxis
Die Studienergebnisse der vergangenen Jahre erlauben – abhängig vom Ischämie- und Blutungsrisiko des Patienten – die Verordnung einer zunehmend individualisierten DAPT nach Stent-Implantation. Entsprechende Scores helfen dabei, das Risiko des einzelnen Patienten besser einschätzen zu können. Künftig könnten zudem Thrombozytenfunktionstests dazu beitragen, die antithrombozytäre Therapie optimal anzupassen.
→Literatur
1. Schomig A, Neumann FJ, Kastrati A, Schuhlen H, Blasini R, Hadamitzky M, Walter H, Zitzmann-Roth EM, Richardt G, Alt E et al: A randomized comparison of antiplatelet and anticoagulant therapy after the placement of coronary-artery stents. N Engl J Med 1996, 334(17):1084-1089.
2. Valgimigli M, Bueno H, Byrne RA, Collet JP, Costa F, Jeppsson A, Juni P, Kastrati A, Kolh P, Mauri L et al: 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2018, 39(3):213-260.
3. Feres F, Costa RA, Abizaid A, Leon MB, Marin-Neto JA, Botelho RV, King SB, 3rd, Negoita M, Liu M, de Paula JE et al: Three vs twelve months of dual antiplatelet therapy after zotarolimus-eluting stents: the OPTIMIZE randomized trial. JAMA 2013, 310(23):2510-2522.
4. Kim BK, Hong MK, Shin DH, Nam CM, Kim JS, Ko YG, Choi D, Kang TS, Park BE, Kang WC et al: A new strategy for discontinuation of dual antiplatelet therapy: the RESET Trial (REal Safety and Efficacy of 3-month dual antiplatelet Therapy following Endeavor zotarolimus-eluting stent implantation). J Am Coll Cardiol 2012, 60(15):1340-1348.
5. Mehran R, Baber U, Steg PG, Ariti C, Weisz G, Witzenbichler B, Henry TD, Kini AS, Stuckey T, Cohen DJ et al: Cessation of dual antiplatelet treatment and cardiac events after percutaneous coronary intervention (PARIS): 2 year results from a prospective observational study. Lancet 2013, 382(9906):1714-1722.
6. Mauri L, Kereiakes DJ, Yeh RW, Driscoll-Shempp P, Cutlip DE, Steg PG, Normand SL, Braunwald E, Wiviott SD, Cohen DJ et al: Twelve or 30 months of dual antiplatelet therapy after drug-eluting stents. N Engl J Med 2014, 371(23):2155-2166.
7. Yeh RW, Kereiakes DJ, Steg PG, Windecker S, Rinaldi MJ, Gershlick AH, Cutlip DE, Cohen DJ, Tanguay JF, Jacobs A et al: Benefits and Risks of Extended Duration Dual Antiplatelet Therapy After PCI in Patients With and Without Acute Myocardial Infarction. J Am Coll Cardiol 2015, 65(20):2211-2221.
8. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C, Horrow J, Husted S, James S, Katus H et al: Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009, 361(11):1045-1057.
9. Wiviott SD, Braunwald E, McCabe CH, Montalescot G, Ruzyllo W, Gottlieb S, Neumann FJ, Ardissino D, De Servi S, Murphy SA et al: Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2007, 357(20):2001-2015.
10. Schupke S, Neumann FJ, Menichelli M, Mayer K, Bernlochner I, Wohrle J, Richardt G, Liebetrau C, Witzenbichler B, Antoniucci D et al: Ticagrelor or Prasugrel in Patients with Acute Coronary Syndromes. N Engl J Med 2019.
11. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK, Clopidogrel in Unstable Angina to Prevent Recurrent Events Trial I: Effects of clopidogrel in addition to ASS in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001, 345(7):494-502.
12. Costa F, van Klaveren D, James S, Heg D, Raber L, Feres F, Pilgrim T, Hong MK, Kim HS, Colombo A et al: Derivation and validation of the predicting bleeding complications in patients undergoing stent implantation and subsequent dual antiplatelet therapy (PRECISE-DAPT) score: a pooled analysis of individual-patient datasets from clinical trials. Lancet 2017, 389(10073):1025-1034.
13. Palmerini T, Della Riva D, Benedetto U, Bacchi Reggiani L, Feres F, Abizaid A, Gilard M, Morice MC, Valgimigli M, Hong MK et al: Three, six, or twelve months of dual antiplatelet therapy after DES implantation in patients with or without acute coronary syndromes: an individual patient data pairwise and network meta-analysis of six randomized trials and 11 473 patients. Eur Heart J 2017, 38(14):1034-1043.
14. Bonaca MP, Bhatt DL, Cohen M, Steg PG, Storey RF, Jensen EC, Magnani G, Bansilal S, Fish MP, Im K et al: Long-term use of ticagrelor in patients with prior myocardial infarction. N Engl J Med 2015, 372(19):1791-1800.
15. Cuisset T, Deharo P, Quilici J, Johnson TW, Deffarges S, Bassez C, Bonnet G, Fourcade L, Mouret JP, Lambert M et al: Benefit of switching dual antiplatelet therapy after acute coronary syndrome: the TOPIC (timing of platelet inhibition after acute coronary syndrome) randomized study. Eur Heart J 2017, 38(41):3070-3078.
16. Sibbing D, Aradi D, Jacobshagen C, Gross L, Trenk D, Geisler T, Orban M, Hadamitzky M, Merkely B, Kiss RG et al: Guided de-escalation of antiplatelet treatment in patients with acute coronary syndrome undergoing percutaneous coronary intervention (TROPICAL-ACS): a randomised, open-label, multicentre trial. Lancet 2017, 390(10104):1747-1757.
17. Antman EM, Wiviott SD, Murphy SA, Voitk J, Hasin Y, Widimsky P, Chandna H, Macias W, McCabe CH, Braunwald E: Early and late benefits of prasugrel in patients with acute coronary syndromes undergoing percutaneous coronary intervention: a TRITON-TIMI 38 (TRial to Assess Improvement in Therapeutic Outcomes by Optimizing Platelet InhibitioN with Prasugrel-Thrombolysis In Myocardial Infarction) analysis. J Am Coll Cardiol 2008, 51(21):2028-2033.
18. Antithrombotic Trialists C, Baigent C, Blackwell L, Collins R, Emberson J, Godwin J, Peto R, Buring J, Hennekens C, Kearney P et al: ASS in the primary and secondary prevention of vascular disease: collaborative meta-analysis of individual participant data from randomised trials. Lancet 2009, 373(9678):1849-1860.
19. Committee CS: A randomised, blinded, trial of clopidogrel versus ASS in patients at risk of ischaemic events (CAPRIE). CAPRIE Steering Committee. Lancet 1996, 348(9038):1329-1339.
20. Connolly SJ, Eikelboom JW, Bosch J, Dagenais G, Dyal L, Lanas F, Metsarinne K, O‘Donnell M, Dans AL, Ha JW et al: Rivaroxaban with or without ASS in patients with stable coronary artery disease: an international, randomised, double-blind, placebo-controlled trial. Lancet 2018, 391(10117):205-218.
21. Eikelboom JW, Connolly SJ, Bosch J, Dagenais GR, Hart RG, Shestakovska O, Diaz R, Alings M, Lonn EM, Anand SS et al: Rivaroxaban with or without ASS in Stable Cardiovascular Disease. N Engl J Med 2017, 377(14):1319-1330.
22. Anand SS, Eikelboom JW, Dyal L, Bosch J, Neumann C, Widimsky P, Avezum AA, Probstfield J, Cook Bruns N, Fox KAA et al: Rivaroxaban Plus ASS Versus ASS in Relation to Vascular Risk in the COMPASS Trial. J Am Coll Cardiol 2019, 73(25):3271-3280.
23. Dans AL, Connolly SJ, Wallentin L, Yang S, Nakamya J, Brueckmann M, Ezekowitz M, Oldgren J, Eikelboom JW, Reilly PA et al: Concomitant use of antiplatelet therapy with dabigatran or warfarin in the Randomized Evaluation of Long-Term Anticoagulation Therapy (RE-LY) trial. Circulation 2013, 127(5):634-640.
24. Hansen ML, Sorensen R, Clausen MT, Fog-Petersen ML, Raunso J, Gadsboll N, Gislason GH, Folke F, Andersen SS, Schramm TK et al: Risk of bleeding with single, dual, or triple therapy with warfarin, ASS, and clopidogrel in patients with atrial fibrillation. Arch Intern Med 2010, 170(16):1433-1441.
25. Oldgren J, Budaj A, Granger CB, Khder Y, Roberts J, Siegbahn A, Tijssen JG, Van de Werf F, Wallentin L, Investigators R-D: Dabigatran vs. placebo in patients with acute coronary syndromes on dual antiplatelet therapy: a randomized, double-blind, phase II trial. Eur Heart J 2011, 32(22):2781-2789.
26. Sorensen R, Hansen ML, Abildstrom SZ, Hvelplund A, Andersson C, Jorgensen C, Madsen JK, Hansen PR, Kober L, Torp-Pedersen C et al: Risk of bleeding in patients with acute myocardial infarction treated with different combinations of ASS, clopidogrel, and vitamin K antagonists in Denmark: a retrospective analysis of nationwide registry data. Lancet 2009, 374(9706):1967-1974.
27. Investigators AWGotA, Connolly S, Pogue J, Hart R, Pfeffer M, Hohnloser S, Chrolavicius S, Pfeffer M, Hohnloser S, Yusuf S: Clopidogrel plus ASS versus oral anticoagulation for atrial fibrillation in the Atrial fibrillation Clopidogrel Trial with Irbesartan for prevention of Vascular Events (ACTIVE W): a randomised controlled trial. Lancet 2006, 367(9526):1903-1912.
28. Cannon CP, Bhatt DL, Oldgren J, Lip GYH, Ellis SG, Kimura T, Maeng M, Merkely B, Zeymer U, Gropper S et al: Dual Antithrombotic Therapy with Dabigatran after PCI in Atrial Fibrillation. N Engl J Med 2017, 377(16):1513-1524.
29. Gibson CM, Mehran R, Bode C, Halperin J, Verheugt FW, Wildgoose P, Birmingham M, Ianus J, Burton P, van Eickels M et al: Prevention of Bleeding in Patients with Atrial Fibrillation Undergoing PCI. N Engl J Med 2016, 375(25):2423-2434.
30. Lopes RD, Heizer G, Aronson R, Vora AN, Massaro T, Mehran R, Goodman SG, Windecker S, Darius H, Li J et al: Antithrombotic Therapy after Acute Coronary Syndrome or PCI in Atrial Fibrillation. N Engl J Med 2019, 380(16):1509-1524.
31. Lamberts M, Gislason GH, Lip GY, Lassen JF, Olesen JB, Mikkelsen AP, Sorensen R, Kober L, Torp-Pedersen C, Hansen ML: Antiplatelet therapy for stable coronary artery disease in atrial fibrillation patients taking an oral anticoagulant: a nationwide cohort study. Circulation 2014, 129(15):1577-1585.
32. Yasuda S, Kaikita K, Akao M, Ako J, Matoba T, Nakamura M, Miyauchi K, Hagiwara N, Kimura K, Hirayama A et al: Antithrombotic Therapy for Atrial Fibrillation with Stable Coronary Disease. N Engl J Med 2019.
Autoren:
 Prof. Dr. med. Stefan Brunner (Foto)
Prof. Dr. med. Stefan Brunner (Foto)
Prof. Dr. med. Steffen Massberg
Klinikum der Universität München, Medizinische Klinik und Poliklinik 1
80336 München
Interessenkonflikte: SB hat ein Beraterhonorar von Bayer erhalten, SM: keine Interessenkonflikte
Weitere Beiträge zu ähnlichen Themen:
Erschienen in: Der Allgemeinarzt, 2020; 42 (4) Seite 22-26