Die Behandlung des Morbus Crohn bedarf einer langfristigen Strategie. An deren Beginn im leichten bis moderaten Stadium bewähren sich die konventionellen Medikamente. Erst danach sieht Prof. Gerhard Rogler, Zürich, den Einsatz für Biologika gerechtfertigt, wie er an der UEG-Week in Barcelona erklärte.
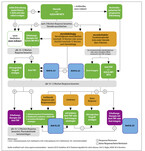
Trotz der mittlerweile großen Auswahl an Biologika sei es wichtig, die Therapie des Morbus Crohn in den Anfangsstadien (bei leichtem Verlauf gegebenenfalls mit hoch dosiertem Mesalazin) mit hoch dosiertem Budesonid (9 mg) oder Kortikosteroiden zu beginnen, eröffnete Prof. Dr. med. Dr. phil. Gerhard Rogler, Direktor der Klinik für Gastroenterologie und Hepatologie, Universitätsspital Zürich, seinen Vortrag. Eine Netzwerkmetaanalyse attestiert diesen drei Substanzen im Vergleich zu Placebo eine gute Wirksamkeit für die Induktion einer Remission bei einem milden bis moderaten Morbus Crohn, wobei das hoch dosierte Budesonid gleich stark wirkt wie Kortikosteroide [1]. Eine Step-up-Therapie scheint wichtig und richtig zu sein, wie eine Auswertung der EPI-IBD-COHORT-Studie nahelegt. In dieser prospektiv laufenden Beobachtungsstudie, an der 31 Zentren in Europa mit 1.289 Patient:innen mit neu diagnostizierter chronisch entzündlicher Darmerkrankung teilnahmen, darunter 488 mit Morbus Crohn, wurde die Erkrankungsaktivität des indolenten Morbus Crohn (n = 97) und der damit einhergehenden Medikation während 28 Monaten beobachtet. 303 Crohn-Patient:innen (62 %) erhielten 5-ASA (5-Aminosalicylsäure) im Verlauf des Beobachtungszeitraums. 97 Patient:innen (20 %) wurden im ersten Jahr nach Diagnose mit 5-ASA behandelt, und 80 Patient:innen (82 %) erhielten gar keine Medikamente. Während des Follow-up benötigten 15 % der indolenten Gruppe mit 5-ASA eine Step-up-Therapie: 4 % im Maximum Kortikosteroide, 12 % Immunmodulatoren und 1 % Biologika. Die meisten Patient:innen (80 %) der indolenten Gruppe und 15 % der gesamten Kohorte benötigten zu keinem Zeitpunkt eine Intensivierung der Therapie. Das bedeutet, dass eine substanzielle Gruppe nur eine milde oder keine Therapie während des Beobachtungszeitraums von 28 Monaten benötigte und einen stillen Krankheitsverlauf durchlebte. Damit bewahre eine gute Patientenstratifizierung nicht nur vor Unter-, sondern auch vor Übertherapie, so das Fazit der Autoren [2]. "Daraus muss man schließen, dass eine Top-down-Strategie für alle Morbus-Crohn-Patienten einer Übertherapie gleichkommt", betonte Rogler. Eine Step-up-Strategie für milde, moderate und schwere chronisch entzündliche Darmerkrankungen fasste er in einem Algorithmus zusammen, der gemeinsam von einer Schweizer Expertengruppe erarbeitet wurde (Abbildung).
Optimieren vor Stufenwechsel
Bevor die nächste Therapiestufe mit Biologika zum Einsatz kommt, empfiehlt Rogler, eine mögliche Verbesserung der bestehenden Therapie durch Optimierung herbeizuführen. Wird beispielsweise Budesonid anstelle von systemischen Kortikosteroiden eingesetzt, sind die steroidabhängigen Nebenwirkungen schwächer [3]. Der Grund: Oral verabreichtes Budesonid weist einen 90 %igen First-Pass-Effekt in der Leber auf und nur 10 % des Wirkstoffs gelangen in den gesamten Körper. Budesonid wirkt also im Darm und wird dann größtenteils in der Leber inaktiviert. Einen Versuch wert sei auch die lokale Verabreichung von Budesonid als Schaum oder Einlauf bei Dickdarm-Crohn, so Rogler, auch wenn beides eigentlich nur bei Colitis ulcerosa zugelassen sei.
Sind Thiopurine im Einsatz, so besteht eine Dosis-Wirkungs-Beziehung [4]. Eine Azathioprin-Standarddosis von 2 bis 2,5 mg/kg kann bei ungenügender Wirkung erhöht werden, so auch die Standarddosis 6-Mercaptopurin 1 bis 1,5 mg/kg. Ein Wirkspiegel von 230 bis 260 pmol Thiopurinmetaboliten (Thioguanin nukleotid, TGN)/8 × 108 Erythrozyten sollte erreicht werden. Werde Aza-
thioprin nicht vertragen, könne auch ein Wechsel auf 6-Mercaptopurin eine Option sein, so Rogler.
Mit der Messung nach vier Wochen lassen sich außerdem Non-Adhärenz, Unterdosierung, Shunting und Wirkungslosigkeit voneinander unterscheiden, sodass die entsprechenden Maßnahmen eingeleitet werden können, ohne erst zwölf Wochen abwarten zu müssen [5].
Auch bei Methotrexat sei eine Dosis-Wirkungs-Beziehung anzunehmen: Dosen unter 15 mg seien bei chronisch entzündlichen Darmerkrankungen ineffektiv, und mehr als die Hälfte der Patient:innen, die mit 15 mg rückfällig würden, könnten mit einer Dosiseskalation auf 25 mg eine anhaltende Remission erreichen, erklärte Rogler. Auch höhere Dosierungen bis zu 35 mg seien möglich, limitierend sei die Verträglichkeit.
Biologika: Mit welchem beginnen?
Weil direkte Vergleichsstudien zur Beantwortung dieser Frage fehlen, muss auf Metaanalysen zurückgegriffen werden, die die Remissionsraten der Biologika miteinander vergleichen.
Bei biologikanaiven Patient:innen ist gemäß einer Netzwerkmetaanalyse die Wahrscheinlichkeit für eine Remission nach Induktion mit Infliximab mit 52,7 % am höchsten. In der Erhaltungstherapie sinkt die Remissionsrate auf 45,7 % aufgrund der Antikörperbildung gegen Infliximab. Die Wahrscheinlichkeiten für eine Remission nach Induktion und Remissionserhalt liegen für Adalimumab bei 41,8 und 57,4 %, für Certolizumab bei 20,5 und 38,3 %, für Vedolizumab bei 33,7 und 37,7 % sowie für Ustekinumab bei 34,2 und 35,8 % [6]. Bei Vedolizumab und Ustekinumab sind die Remissionsraten über die ganze Therapie konstant.
Bei Patient:innen mit moderatem bis schwerem Morbus Crohn und Biologikaerfahrung beziehungsweise bereits erfolgter Anti-TNF-Therapie (meist Infliximab) scheint die Remissionsinduktion unter Adalimumab und Ustekinumab gemäß einer weiteren Netzwerkmetaanalyse am aussichtsreichsten zu sein [7].
Bei etwa einem Drittel der Patient:innen tritt unter einem Anti-TNF im Therapieverlauf ein Responseverlust auf. In diesem Fall besteht mit einer Optimierung beziehungsweise einer Intervallverkürzung gemäß Rogler eine realistische Chance auf eine Wiedererlangung der Wirkung [8].
Was sollte das Ziel einer Behandlung sein?
Die klinische Remission kann ein realistisches Ziel sein. Die Mukosaheilung als Remissionsziel, wie in vielen Studien verwendet, wird gemäß Rogler mit Biologika nur selten erreicht. Nach einer chirurgisch induzierten Remission dagegen sei es das Ziel, einen Rückfall zu verhindern. Hier habe in einer kürzlich publizierten Cochrane-Netzwerkmetaanalyse von 20 randomisiert kontrollierten Studien 5-ASA die beste Evidenz für eine Rückfallprävention gezeigt [9], so Rogler abschließend.
- Bei M. Crohn sollte man die Therapie beginnen mit Mesalazin, Budesonid oder Kortikosteroiden.
- Besser step-up statt step-down. Step-down für alle Patient:innen würde eine Übertherapie bedeuten.
- Vor dem Einsatz von Biologika Therapie optimieren!
Quelle: "Therapy update: Practical algorithms in Crohn’s disease – optimization when possible"; United European Gastroenterology Week (UEGW) 2019, 21. bis 23. Oktober in Barcelona
Genehmigter und bearbeiteter Nachdruck aus Ars medici Dossier VI + VII, 2020
Erschienen in: doctors|today, 2021; 1 (8) Seite 52-54