Diabetes mellitus ist mit der Entwicklung von chronischen Folgeerkrankungen assoziiert, die sich langfristig nicht nur auf die Lebensqualität, sondern auch auf die Lebenserwartung auswirken. Zu den häufigen Komorbiditäten von Diabetes gehören kardiovaskuläre Erkrankungen wie die Herzinsuffizienz.
Patienten, die unter Herzinsuffizienz leiden, werden entsprechend der linken ventrikulären Ejektionsfraktion (LVEF) einer von drei Kategorien zugeordnet: Herzinsuffizienz mit erhaltener (HFpEF; LVEF ≥ 50 %), mittlerer (HFmEF; LVEF 41–49 %) und reduzierter (HFrEF; LVEF ≤ 40 %) Ejektionsfraktion [2, 3].
Das Vorliegen eines Diabetes ist ein eigenständiger Risikofaktor für die Entwicklung von Herzinsuffizienz. Patienten mit Diabetes entwickeln 2- bis 5-mal häufiger und in jüngeren Lebensjahren eine Herzinsuffizienz [4, 5, 6, 7]. Bis zu 30 % aller Patienten mit Diabetes haben eine Herzinsuffizienz [8, 9]. Davon wiesen nahezu 30 % eine HFpEF und circa 5 % eine HFrEF auf [8]. Umgekehrt ist das Vorliegen einer Herzinsuffizienz ein Risikofaktor für die Entwicklung eines Diabetes [10, 11, 7]. Etwa 30–40 % aller Patienten mit Herzinsuffizienz haben einen Prädiabetes oder einen manifestierten Diabetes [12, 9].
Das gemeinsame Vorliegen eines Diabetes und einer Herzinsuffizienz verschlechtert die Prognose der Patienten signifikant. Es erhöht das Risiko für herzinsuffizienzbedingte Hospitalisierungen und ist mit einer höheren kardiovaskulären und allgemeinen Mortalitätsrate assoziiert [13, 12, 14, 15]. Die frühzeitige Erkennung und konsequente Behandlung von Diabetes und seinen Begleiterkrankungen, wie Herzinsuffizienz, besitzen daher hohe Priorität.
Diagnostik von Herzinsuffizienz mit Biomarkern
In den vergangenen Jahren ist die Bestimmung von zirkulierenden Biomarkern zur frühzeitigen Erkennung einer Herzinsuffizienz mehr und mehr in den Vordergrund der klinischen Diagnostik gerückt. Hierzu gehören natriuretische Peptide (NT-proBNP und BNP). Erhöhte Plasmakonzentrationen der natriuretischen Peptide korrelieren mit dem Schweregrad der Herzinsuffizienz und einem höheren Mortalitätsrisiko und eignen sich daher über die Diagnose hinaus auch zu prognostischen Zwecken, insbesondere bei Patienten mit Diabetes [16, 17].
Natriuretische Peptide: Empfehlungen aus Konsensuspapieren von 2022
DGK/DDG-Positionspapier 2022
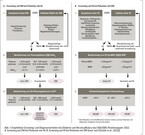
Die Deutsche Gesellschaft für Kardiologie (DGK) und die Deutsche Diabetes Gesellschaft (DDG) empfehlen in einem aktuellen Positionspapier [9] sowohl ein Screening auf Diabetes bei Patienten mit Herzinsuffizienz als auch umgekehrt, um das mögliche gemeinsame Vorliegen beider Erkrankungen frühzeitig erkennen zu können (Abb. 1). Patienten mit einer Herzinsuffizienz sollten auf Diabetes gescreent werden, wenn Symptome eines Diabetes vorliegen oder ein erhöhtes Diabetes-Risiko besteht (Abb. 1A). Bei einem positiven Befund wird eine gleichzeitige Messung von Plasmaglukose und HbA1c-Wert empfohlen. Eine Diabetes-Diagnose kann ab einer Plasmakonzentration von ≥ 126 mg/dl (≥ 7,0 mmol/l) und einem HbA1c-Wert von ≥ 6,5 % gestellt werden. In den Graubereich fallen Patienten mit einer Plasmaglukose von 100–125 mg/dl (5,6–6,9 mmol/l) und/oder einem HbA1c-Wert von 5,7–6,4 %. Als sicherer Nachweis eines Diabetes gilt eine 2-Stunden-Plasmaglukose von ≥ 200 mg/dl (≥ 11,1 mmol/l).
Patienten mit einem vorhandenen Diabetes sollten aufgrund des hohen Risikos für eine Herzinsuffizienz bei jedem ärztlichen Besuch auf das Vorliegen von Symptomen oder Zeichen einer Herzinsuffizienz gescreent werden (Abb. 1B). Sobald Verdacht auf eine Herzinsuffizienz besteht, sollte eine Bestimmung der natriuretischen Peptide durchgeführt werden. Bei einem NT-proBNP < 125 pg/ml und BNP < 35 pg/ml ist eine Herzinsuffizienz unwahrscheinlich, wobei bei Patienten mit Vorhofflimmern höhere Grenzwerte (NT-proBNP < 365 pg/ml und BNP < 105 pg/ml) gelten. Patienten mit Adipositas können hingegen falsch-niedrige Werte aufweisen und dennoch einem hohen Herzinsuffizienzrisiko ausgesetzt sein [18]. Bei einer über dem Grenzwert liegenden Plasmakonzentration der natriuretischen Peptide sollte eine unmittelbare Vorstellung beim Kardiologen erfolgen. Hier sollte mittels Echokardiographie die zugrundeliegende Ätiologie der Herzinsuffizienz geklärt werden, um mögliche reversible oder behandelbare Ursachen zu bestimmen.
ADA-Konsensuspapier 2022
Einem aktuellen Konsensuspapier der American Diabetes Association (ADA) folgend werden Patienten entsprechend ihrem Risiko und den Symptomen einer Herzinsuffizienz in die Stadien A, B oder C/D eingeteilt [19]. Patienten, die ein hohes Risiko für die Entwicklung einer Herzinsuffizienz aufweisen, werden dem Stadium A zugeordnet. Grundsätzlich fallen alle Patienten mit einem manifestierten Diabetes automatisch in dieses Stadium, wenn sie mindestens einen Risikofaktor, wie z. B. Adipositas, aufweisen. Dem Stadium B werden Patienten zugeordnet, die eine strukturelle und/oder funktionelle kardiale Anomalie oder bereits erhöhte Werte an Biomarkern (NT-proBNP, BNP oder hs-cTN) aufweisen, aber (noch) keine Symptome einer Herzinsuffizienz zeigen. Ein Großteil der Patienten mit Diabetes fällt in dieses Stadium [20, 21]. Sowohl Patienten im Stadium A als auch Stadium B sollten mindestens einmal jährlich ein Biomarker-Screening durchführen. Die Grenzwerte für die Biomarker liegen laut ADA bei NT-proBNP ≥ 125 pg/ml, BNP ≥ 50 pg/ml. Wichtig ist, dass bei Patienten in einem höheren Alter, mit einer fortgeschrittenen chronischen Nierenerkrankung oder mit Vorhofflimmern höhere Grenzwerte und bei Patienten mit Adipositas geringere Grenzwerte gelten können. Bei erhöhten Werten sollte eine echokardiographische Abklärung folgen. Patienten mit früheren oder aktuellen Symptomen einer Herzinsuffizienz werden dem Stadium C/D zugeordnet. Diese sollten gründlich auf Zeichen einer Herzinsuffizienz untersucht werden und bildgebenden Verfahren unterzogen werden. Die Echokardiographie ist eine besonders geeignete Methode, um eine Diagnose und die klinischen Ursachen einer Herzinsuffizienz definieren zu können. Diese liefert Informationen zu den kardialen strukturellen und funktionellen Veränderungen, erlaubt eine Schlussfolgerung über die Ätiologie und ermöglicht eine Differenzierung zwischen einer HFpEF und HFrEF.
Fazit
Diabetes und Herzinsuffizienz stellen gegenseitige Risikofaktoren dar und das Vorliegen beider Erkrankungen verschlechtert die Prognose der Patienten signifikant. Daher sollten Patienten regelmäßig auf die jeweils andere Erkrankung gescreent werden. Die aktuellen Konsensuspapiere der DGK/DDG und ADA fassen klare Anleitungen für das Screeningverfahren von Patienten mit Diabetes oder Herzinsuffizienz zusammen. Sie liefern definierte Grenzwerte für die natriuretischen Peptide, die als zirkulierende Biomarker eine frühe Diagnose einer Herzinsuffizienz erlauben. Differenzierte therapeutische Interventionen bei gleichzeitiger Vermeidung der Medikamentenklassen, die das herzinsuffizienzbedingte Hospitalisierungsrisiko erhöhen, werden empfohlen, um die langfristige Prognose von Patienten mit Diabetes und Herzinsuffizienz zu verbessern.
- Das Vorliegen eines Diabetes gilt als unabhängiger Risikofaktor für die Entwicklung einer Herzinsuffizienz und umgekehrt.
- Das gleichzeitige Auftreten von Diabetes und Herzinsuffizienz ist mit einem höheren Hospitalisierungs- und Mortalitätsrisiko assoziiert. Daher sollten Patienten mit Diabetes oder Herzinsuffizienz regelmäßig auf die jeweils andere Erkrankung untersucht werden.
- Die aktuellen Empfehlungen des DGK/DDG-Positionspapiers 2022 und des ADA-Konsensuspapiers 2022 unterstreichen natriuretische Peptide, wie zum Beispiel NT-proBNP, als geeignete Biomarker für die Diagnose und die Beurteilung der Prognose einer Herzinsuffizienz.
Prof. Dr. Oliver Schnell
Erschienen in: doctors|today, 2023; 3 (4) Seite 34-36