Sollte man Menschen, die bereits einen Herpes zoster durchgemacht haben, mit dem vom RKI empfohlenen Totimpfstoff Shingrix® impfen? Möglich ist es, doch zum besten Zeitpunkt und zur Wirksamkeit der Impfung in dieser Situation ist die Datenlage noch recht dünn. Auf jeden Fall sollte man die individuelle Situation der Patient:in berücksichtigen.
Im Frühjahr 2018 wurde ein adjuvantierter rekombinanter Herpes-zoster(HZ)-Totimpfstoff zum Schutz vor Herpes zoster und postherpetischer Neuralgie zunächst für Personen ab einem Alter von 50 Jahren zugelassen. Die Ergebnisse der Zulassungsstudien belegen die hohe Effektivität des Impfstoffs bei über 50-jährigen Erwachsenen [1] und bei über 70-Jährigen [2]. Die Impfserie besteht aus zwei Impfstoffdosen, die intramuskulär (i.m.) im Abstand von zwei bis sechs Monaten verabreicht werden (Fachinformation Shingrix®, Stand September 2021).
Die Ständige Impfkommission (STIKO) empfiehlt die Impfung als Standardimpfung für alle Menschen im Alter von über 60 Jahren. Zusätzlich wird die Impfung als Indikationsimpfung für Personen im Alter von über 50 Jahren mit einer Grunderkrankung oder einer angeborenen bzw. erworbenen Immunschwäche empfohlen [3].
Im August 2020 wurde die Zulassung auf Erwachsene im Alter von über 18 Jahren mit einer Grunderkrankung, welche das Risiko für einen Herpes zoster erhöht, erweitert.
Impfung von HIV-Patient:innen
In den Hinweisen der Ständigen Impfkommission — die "Anwendungshinweise" gehen speziell auf Impfungen für immunsupprimierte Patient:innen ein — wird die Impfung von über 18 Jahre alten HIV-infizierten Personen empfohlen [4]. Bei der Indikationsstellung zur Herpes-zoster-Impfung sind bei Menschen mit HIV-Infektion der Erfolg einer antiretroviralen Therapie sowie immunologische Parameter wie die CD4-Zellzahl und die CD4/CD8-Ratio zu berücksichtigen. Auch bei jüngeren HIV-infizierten Erwachsenen mit niedrigen CD4-Zellen und schlechtem immunologischem Ansprechen auf eine antiretrovirale Therapie kann eine Zoster-Impfung indiziert sein. Das in dem Herpes-zoster-Totimpfstoff enthaltene Adjuvans (AS01) verstärkt die CD4-T-Zell-vermittelte und die humorale Immunantwort. Damit kann der Impfstoff auch bei Personen, bei denen das Immunsystem suboptimal arbeitet, eine starke zellvermittelte Immunantwort induzieren.
Herpes-zoster-Rezidive
Es wird geschätzt, dass ca. 5 % aller immunkompetenten Patient:innen, die an einem Herpes zoster erkrankt waren, ein Rezidiv erleiden [5]. Jedoch fehlen Studien, bei denen die Rezidive diagnostisch mittels PCR abgesichert wurden.
Man nimmt an, dass eine Herpes-zoster-Erkrankung zu einer "Boosterung" sowohl der zellulären als auch der humoralen Immunität führt [6]. Patient:innen mit Immundefizienz sind dabei nach einer Herpes-zoster-Erkrankung — abhängig von Art und Ausmaß des Immundefekts — wahrscheinlich deutlich kürzer vor einer erneuten Erkrankung geschützt als immunkompetente Menschen.
Patient:innen mit bestimmten Grunderkrankungen (z.B. Asthma bronchiale, koronare Herzkrankheit (KHK), chronisch-obstruktive Lungenerkrankung (COPD), Depression, rheumatoide Arthritis) haben ein deutlich höheres Risiko, nach einer Herpes-zoster-Erkrankung innerhalb der folgenden zehn Jahre ein Rezidiv zu erleiden. Wie Abbildung 1 auf der Folgeseite zeigt, haben Betroffene unter 60 Jahren mit mindestens einer Grunderkrankung interessanterweise ein höheres Rezidivrisiko als ältere (≥ 60-jährige) Patient:innen. Im Durchschnitt tritt das erste Rezidiv 4,7 Jahre nach einer Herpes-zoster-Erkrankung auf. HIV-infizierte Menschen haben ein 15-fach erhöhtes Risiko [7]. Dieses nimmt unter antiretroviraler Therapie im Rahmen der Immunrekonstitution ab, ist aber weiter erhöht [8]. Noch höher ist das Rezidivrisiko nach einer Stammzelltransplantation: Bis zu 30% der Transplantierten erleiden ein Herpes-zoster-Rezidiv.
Die Datenlage zur Impfung von Personen, die an einem Herpes zoster erkrankt waren, ist derzeit begrenzt: Im Rahmen der nicht randomisierten Phase-III-Studie "Zoster-033" wurden 96 Erwachsene ≥ 50 Jahre mit einer ärztlich diagnostizierten und ausgeheilten Herpes-zoster-Erkrankung mit zwei Dosen des HZ-Totimpfstoffs Shingrix® im Abstand von zwei Monaten geimpft [9]. Eine virol. Bestätigung mittels PCR erfolgte nicht. Die Antikörpertiter (Anti-gE GMC) wurden einen Monat nach der zweiten Impfdosis bestimmt. Sie waren nach den beiden Impfungen signifikant angestiegen. Innerhalb von einem Jahr nach der Impfung wurden bei sechs Patient:innen insgesamt neun Verdachtsfälle eines Herpes zoster gemeldet. Diese Zahl ist höher, als es bei Ungeimpften, die an Herpes zoster erkrankt waren, zu erwarten wäre. Alle Verdachtsfälle von Herpes-zoster-Rezidiven nach der Impfung wurden von teilnehmenden Studienzentren in Kanada gemeldet, während aus den russischen Zentren keine Verdachtsfälle bekannt wurden. Es war in dieser Studie allerdings nicht vorgesehen, dass der Verdacht ärztlicherseits bestätigt werden musste. Möglicherweise handelte es sich nicht bei allen gemeldeten Verdachtsfällen um einen Herpes zoster.
In einer laufenden Placebo-kontrollierten Studie (Zoster 062 Hz/su) werden nur Patient:innen mit einer einzigen Herpes-zoster-Episode eingeschlossen [11]. Sofern der Verdacht auf eine Herpes-zoster-Erkrankung besteht, wird die Diagnose mittels PCR aus dem Bläscheninhalt bestätigt oder — bei negativer PCR — eine altern. Diagnose in Betracht gezogen. Erste Ergebnisse werden 2024 vorliegen.
Impfung nach einer Herpes-zoster-Episode
Zu der Fragestellung "Zeitpunkt der Impfung nach stattgehabtem Herpes zoster" existieren keine prospektiven randomisierten Studien. Daher beruhen die verschiedenen Empfehlungen auf den Expertenmeinungen der nationalen Impfkommissionen.
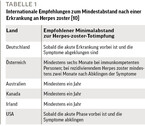
Die Ständige Impfkommission (STIKO) beim RobertKoch-Institut führt in ihrer aktuellen Publikation zur Impfung von Patient:innen, die bereits an einem Herpes zoster erkrankt waren, aus: "Die HZ-Impfung mit dem Totimpfstoff können auch Personen bekommen, die bereits in der Vergangenheit an HZ erkrankt waren. Der Herpes zoster ist allerdings nicht zur Therapie einer HZ-Erkrankung oder ihrer Spätfolgen bestimmt. Auf Basis einer Studie bei ≥50-Jährigen ist der Impfstoff nach vorausgegangener HZ-Erkrankung ausreichend immunogen und sicher. Die Datenlage zur klinischen Wirksamkeit bei Anwendung des Impfstoffs und zum günstigsten Zeitpunkt der Impfung nach HZ-Erkrankung ist begrenzt. Die Impfung sollte daher zu einem Zeitpunkt erfolgen, wenn die akute Erkrankung vorüber ist und die Symptome abgeklungen sind." Nach der Empfehlung der STIKO kann die Impfung also direkt nach Abklingen der Symptome erfolgen.
Diese Empfehlung wird auch von den Centers for Disease Control (CDC, USA) ausgesprochen [12, 13].
Das "Nationale Impfgremium" der Republik Österreich (Bundesministerium für Arbeit, Soziales, Gesundheit und Konsumentenschutz/BMASGK) empfiehlt dagegen, frühestens sechs Monate nach einer Herpes-zoster-Erkrankung zu impfen [14].
Das Department for Health and Aged Care der australischen Regierung rät, frühestens ein Jahr nach durchgemachter Herpes-zoster-Erkrankung gegen Herpes zoster zu impfen, da bis dahin ein Schutz durch die überstandene Erkrankung besteht [15].
Die irische Leitlinie empfiehlt ebenfalls, nach überstandener Herpes-zoster-Erkrankung frühestens nach einem Jahr zu impfen [16].
Ergebnisse eines Expertenworkshops in Potsdam
Eine Expertenrunde aus den Bereichen Mikrobiologie, Virologie und Infektionsepidemiologie, Innere Medizin, Infektiologie, Onkologie, Rheumatologie/Immunologie, Geriatrie, Dermatologie sowie Kinderheilkunde hat die Vor- und Nachteile der unterschiedlichen Impfzeitpunkte intensiv diskutiert. Generell gilt, dass es sich nicht um eine Ausschließlichkeitsempfehlung handelt und die Impfstrategie die individuelle Situation der Patient:innen berücksichtigen sollte. So ist es zum Beispiel sinnvoll, bei Tumorpatient:innen das Ende einer Chemotherapie abzuwarten, bevor die Impfung erfolgt. Impfungen sollen auch generell möglichst nicht während einer aktiven Phase einer Autoimmunerkrankung durchgeführt werden: Die laufende (Auto-)Immunreaktion selbst und die immunsuppressive Therapie beeinträchtigen den Impferfolg.
Je früher die Impfung nach einer Erkrankung durchgeführt wird, desto unwahrscheinlicher ist es, dass die Impfung vergessen wird: Viele Patient:innen sind kurz nach der häufig sehr schmerzhaften Erkrankung hoch motiviert, sich gegen ein Rezidiv impfen zu lassen. Um einen möglichst langanhaltenden Immunschutz zu erhalten, ist es allerdings aus immunologischer Sicht sinnvoll, mindestens 6 – 8 Wochen nach der Erkrankung zu warten, bis diese abgeklungen ist, bevor eine erneute Immunaktivierung mit dem gleichen Antigen (Impfung) erfolgt. Daher erscheint ein Mindestabstand zur Impfung von 6 – 8 Wochen nach Abklingen der akuten Symptome eines HZ sinnvoll. Aber auch bei Impfung unmittelbar nach Abklingen der Symptome bestehen nach der aktuellen Datenlage keine Sicherheitsbedenken. Aus medizinischen Gründen ist eine frühe Impfung – ca. 2 – 3 Monate nach einem vorausgegangenen HZ –besonders bei Patient:innen vorzuziehen, die auf längere Sicht erheblich immunsupprimiert sind, weil diese vermutlich ein höheres Risiko für frühe Rezidive haben.
Für eine Impfung früh nach der Abheilung sprechen:
- Die Patient:in ist in der Regel noch motiviert, da die Erkrankung erst kurz zurückliegt.
- Bei Hochrisikopatient:innen für ein frühes HZ-Rezidiv kann dieses durch die Impfung wahrscheinlich verhindert werden.
Für eine Impfung mit zeitlichem Abstand sprechen:
- Rezidive treten bei Immunkompetenten sehr selten vor Ablauf eines Jahres (im Durchschnitt nach 4,7 Jahren) auf.
- Die Bildung von T-Gedächtnis-Lymphozyten ist nach einer Virusinfektion erst nach ca. 6 – 8 Wochen abgeschlossen.
Die erarbeiteten Empfehlungen lauten [17]:
- "Nach überstandener Herpes-zoster-Erkrankung sollte eine Impfung mit zwei Impfdosen des rekombinanten Herpes-zoster-Impfstoffs erfolgen."
- "Die Impfung sollte nach Möglichkeit im Zeitraum von 3 bis 12 Monaten nach der Erkrankung erfolgen."
- "Die Impfung kann gleichzeitig mit anderen Impfungen wie zum Beispiel der Influenza-Impfung oder der Impfung gegen Pneumokokkeninfektionen durchgeführt werden."
- "Wenn die Impfung nicht innerhalb des ersten Jahres nach der Erkrankung durchgeführt wurde, sollte sie zum frühestmöglichen Zeitpunkt nachgeholt werden."
- "Die Erkrankung muss zum Zeitpunkt der ersten Impfung vollständig abgeheilt sein."
- "Der Impfzeitpunkt sollte den individuellen Gegebenheiten angepasst werden, unter anderem nicht während eines Schubes einer Autoimmunerkrankung, möglichst nach Beendigung bzw. Dosisreduktion immunsuppressiver Behandlungen (z. B. Chemotherapie von Tumorerkrankungen). Bei erheblich immunsupprimierten Patienten mit Risikofür ein Frührezidiv des HZ frühzeitige Impfung bevorzugen (z. B. nach 3 Monaten)."
- Die Erkrankung muss zum Zeitpunkt der ersten Impfung vollständig abgeheilt sein.
- Die Impfung sollte wenn möglich im Zeitraum von 3 bis 12 Monaten nach der Erkrankung erfolgen.
- Geimpft werden kann gleichzeitig mit anderen Tot-Impfungen wie z. B. der Influenza-Schutzimpfung.
- Dr. med. Andreas Leischker, Lehrbeauftragter an der Phillips Universität Marburg, 35037 Marburg
- Priv.Doz. Dr. Stefan Esser, Klinik für Dermatologie, Universitätsklinikum Essen, 45122 Essen
- Prof. Dr.Matthias Goebler, FA für Dermatologie und Venerologie, Direktor der Klinik und Poliklinik für Dermatologie,Venerologie und Allergologie, Universitätsklinikum Würzburg
- Prof .Dr. Daniela Huzly,FÄ für Mikrobiologie, Virologie und Infektionsepidemiologie, Institut für Virologie,Universitätsklinikum Freiburg
- Dr. Wolfgang Kreischer, Facharzt für Allgemeinmedizin, Praxis Dr. Kreischer und Kollegen,Clayallee177,14195 Berlin
- Prof. Dr.Thomas Weinke, FA für Innere Medizin ,Gastroenterologie ,Tropenmedizin Zentrum für Innere Medizin, Klinik für Gastroenterologie,Infektiologie und Tropenmedizin, Klinikum Ernst von Bergmann, Potsdam
- Prof Dr. Clemens Wendtner, Klinik für Hämatologie, Onkologie, Immunologie, Palliativmedizin, Infektiologie und Tropenmedizin, München Klinik Schwabing, Akademisches Lehrkrankenhaus der Ludwig-Maximilians-Universität (LMU), München
- Prof. Dr. Reinhard Voll, Ärztlicher Direktor Klinik für Rheumatologie und Klinische Immunologie Universitätsklinikum Freiburg, 79106 Freiburg
- Dr. med. Til R. Kiderlen Chefarzt für Hämatologie, Onkologie und Palliativmedizin, DRK Kliniken Berlin Köpenick, 12559 Berlin
- A. Leischker: Honorare für Vorträge und Beratungstätigkeiten von Centrum für Reisemedizin Düsseldorf, Sanofi, GlaxoSmithKline (GSK), Pfizer Vaccines, Novartis und Takeda
- C. Wendtner: Reiseunterstützung/Travel grants sowie Beratungshonorare/Advisory Boards seitens GSK
- S. Esser: Beratungs-bzw. Gutachtertätigkeit (Advisory Boards): Abbvie, Gilead, GSK, Janssen, MSD, ViiV. 5. Honorare: Abbvie, Gilead, Janssen, MSD, ViiV., Finanzierung wissenschaftlicher Untersuchungen: Gilead, Janssen, MSD, ViiV, andere finanzielle Beziehungen (Reisekosten): Abbvie, Gilead, Janssen, MSD, ViiV.
Erschienen in: doctors|today, 2023; 3 (1) Seite 30-33