Die typischen Symptome einer diabetischen Neuropathie, wie Missempfindungen und Schmerzen in den Extremitäten, schränken die Lebensqualität der Betroffenen erheblich ein. Darüber hinaus erhöht die Erkrankung das Risiko für Komplikationen sowie die Mortalität. Leider wird die Neuropathie oft spät erkannt. Aktuelle Empfehlungen zur Diagnostik und Therapie erleichtern das Management der Erkrankung in der Praxis. Die Therapie sollte auf drei Säulen ruhen: der kausalen Behandlung (z. B. Blutzuckereinstellung), der pathogenetisch orientierten Pharmakotherapie (z. B. Benfotiamin, Alpha-Liponsäure) und der symptomatischen Therapie.
- das autonome Nervensystem und/oder
- das somatische Nervensystem betreffen.
Beide Formen der diabetischen Neuropathie gehen nicht nur mit einer deutlich verringerten Lebensqualität einher, sondern korrelieren auch mit einem erhöhten Risiko für weitere Komplikationen und einer erhöhten Mortalität. Bei Diabetiker:innen mit kardiovaskulärer autonomer diabetischer Neuropathie (KAN) – Kennzeichen sind u. a. Ruhetachykardie, reduzierte Herzfrequenzvariabilität und orthostatische Hypotonie – ist das Sterberisiko im Vergleich zu Patient:innen ohne KAN im Verlauf von bis zu 15 Jahren um den Faktor 3,5 erhöht [3].
Die distal-sensomotorische Polyneuropathie (DSPN), die etwa drei Viertel aller diabetischen Neuropathien ausmacht, kann die Lebensqualität der Betroffenen durch quälende Schmerzen und Missempfindungen in den unteren Extremitäten erheblich beeinträchtigen. 13 bis 26 % der Diabetiker:innen leiden unter einer schmerzhaften Form der Erkrankung [3]. In bis zu 50 % der Fälle kann die DSPN aber auch asymptomatisch verlaufen [4]. Aus diesem Grund wird die Diagnose häufig erst mit großer Verzögerung gestellt. Die DSPN ist aber auch von größter Relevanz als Risikofaktor für ein diabetisches Fußsyndrom (DFS). In 85 bis 90 % der Fälle ist die Nervenschädigung an der Ätiologie des DFS beteiligt und hat damit einen erstrangigen Stellenwert in der Risikokonstellation für Fußulkus und Amputation [3].
Typische Beschwerden im Rahmen der DSPN sind:
- Neuropathische Symptome in den Extremitäten (vor allem in den Füßen, seltener in den Händen) wie einschießende oder stechende Schmerzen, Kribbeln, "Ameisenlaufen", Brennen, Krämpfe, Kälte- oder Taubheitsgefühl, Schmerzen bei einfacher Berührung, z. B. mit der Bettdecke.
- Neuropathische Defizite ("negative Symptome"), die von Patient:innen lange Zeit nicht bemerkt werden, wie Abnahme der Warm-/Kalt-, Berührungs- oder Vibrationsempfindung bzw. der Schmerzempfindung.
Trotz der gravierenden Auswirkungen der DSPN auf Lebensqualität, Morbidität und Mortalität bestehen große Defizite bei der Diagnostik der DSPN. In der PROTECT-Studie mit 1.850 Teilnehmer:innen, darunter 943 Typ-2-, 126 Typ-1- und 781 Nicht-Diabetiker:innen, wussten fast 70 % der Teilnehmer:innen eines Neuropathie-Screenings, bei denen eine Neuropathie nachgewiesen wurde, zuvor nichts von einer Erkrankung der peripheren Nerven. Selbst von den Befragten, die Schmerzen oder Brennen in den Füßen als Beschwerden angaben, war die Ursache dafür zwei Dritteln nicht bekannt [12].
Rund ein Viertel bis 30 % der Teilnehmer:innen mit nachgewiesener DSPN hatten eine schmerzlose Verlaufsform, rund 15 % eine atypische DSPN mit Schmerzen nur beim Gehen [13]. Parästhesien bzw. Taubheitsgefühl an den Füßen waren die häufigsten Symptome, Schmerzen nahmen in der Regel mit dem Schweregrad der Neuropathie zu. Daten wie die Ergebnisse des KORA-S-4-Surveys weisen auch auf eine deutliche Unterversorgung in der Therapie hin: Lediglich 38 % der Personen mit schmerzhafter DSPN erhielten Schmerzmittel und nur 6 % der Teilnehmer:innen mit DSPN eine Pharmakotherapie gegen die Neuropathie [14].
Um das Management der DSPN in der Praxis zu erleichtern, wurde aktuell von 15 internationalen Neuropathie-Expert:innen ein Konsensuspapier mit Empfehlungen zum Screening, zur Diagnose und Therapie der DSPN veröffentlicht [1].
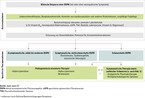
Das Expertengremium weist darauf hin, dass meist sowohl die kleinen als auch die großen Nervenfasern geschädigt sind. Deshalb sollten bei einem Screening auf DSPN geeignete Tests zur Beurteilung unterschiedlicher Nervenfasertypen eingesetzt werden (Abb. 1).
Screening und Diagnostik
Da eine diabetische Neuropathie keineswegs eine Spätkomplikation des Diabetes mellitus ist [5], sollte das Screening frühzeitig erfolgen. Zum Zeitpunkt der Diabetesdiagnose besteht bei einigen Typ-2-Diabetes-Patient:innen schon jahrelang eine Hyperglykämie und/oder gestörte Glukosetoleranz. Daher kann eine diabetische Neuropathie bereits zum Zeitpunkt der Diabetesdiagnose präsent sein. In einer Studie wurde bei jeder vierten älteren Person mit Prädiabetes eine diabetische Neuropathie (DSPN) nachgewiesen [6]. Insbesondere bei gleichzeitigem Vorliegen einer gestörten Nüchternglukose und Glukosetoleranz ist die Prävalenz einer DSPN und einer KAN erhöht [7].
Von der Deutschen Diabetes Gesellschaft wird ein Screening auf eine DSPN und/oder KAN bei Patient:innen mit Typ-2-Diabetes zum Zeitpunkt der Diabetesdiagnose und bei Patient:innen mit Typ-1-Diabetes spätestens fünf Jahre nach Diagnosestellung empfohlen [3].
Zum Screening auf DSPN gehören eine Anamnese, Inspektion und klinische Untersuchung der Füße, Erfassung der neuropathischen Symptome und Defizite sowie einfache neurologische Tests (Abb. 1). Als einfaches Screeningtool zur Erstabklärung neuropathischer Schmerzen wird im Konsensuspapier der DN4-Fragebogen (Douleur Neuropathique en 4 Questions) empfohlen [1]. Neuropathische Schmerzen nehmen typischerweise während der Nacht zu und können sowohl den Schlaf als auch die Tagesaktivitäten beeinträchtigen. Zur Beurteilung der Intensität neuropathischer Schmerzen kann die numerische 11-Punkt-Likert-Skala oder eine visuelle Analogskala eingesetzt werden. Generell ist die Anwendung validierter Neuropathie-Scores und -Fragebögen wichtig, um neuropathische Symptome und Defizite zu erfassen und zu bewerten.
- Diabetesdauer
- Diabeteseinstellung (Hyperglykämie)
- arterielle Hypertonie
- periphere arterielle Verschlusskrankheit (pAVK)
- Mediasklerose vom Typ Mönckeberg
- diabetische Retino- und Nephropathie
- Depression
- viszerale Adipositas
- Hyperlipidämie
- Alkohol, Nikotin
- mangelnde körperliche Aktivität
- demografische Faktoren (Alter, Körpergröße, Körpergewicht)
Als Minimalkriterium für die Diagnose einer DSPN in der klinischen Praxis einigte sich die Expertengruppe auf den Nachweis einer beidseitigen Verschlechterung des Vibrationsempfindens der unteren Extremitäten, z. B. beurteilt mit der RydelSeiffer-Stimmgabel (große Nervenfasern), und/oder des Schmerzempfindens (kleine Nervenfasern). Empfohlen wird die Messung des Vibrationsempfindens dorsal auf der Großzehe. Dabei sollten altersabhängige Grenzwerte berücksichtigt werden [1].
Für die Beurteilung des Druck- und Berührungsempfindens wird ein Test mit dem 10 g Monofilament empfohlen, alternativ kann z. B. ein Q-Tip verwendet werden. Ein auffälliger Test auf dem Rücken der Großzehe liefert Hinweise für eine DSPN, ein auffälliges Ergebnis an der Fußsohle weist zudem auf ein erhöhtes Risiko einer Fußulzeration hin.
Zur Beurteilung der Funktion der kleinen Nervenfasern werden primär Testungen des Schmerzempfindens des Fußes (mit NeurotipsTM/Neuropen®, Pinprick oder Ähnlichem) sowie des Temperaturempfindens (mit Tip Therm®, einer kalten Stimmgabel oder Ähnlichem) empfohlen. Wer über entsprechende Geräte verfügt, kann zusätzlich zur Beurteilung der autonomen Nervenfunktion die Schweißproduktion oder die elektrochemische Leitfähigkeit der Haut messen [1]. Zur Erfassung einer KAN sind laut Praxisempfehlungen der DDG mindestens zwei autonome Reflextests erforderlich: die Herzfrequenzvariabilität sowie der Orthostase-Test [3].
Bei allen Patient:innen mit pathologischen Testergebnissen, auffälligen anamnestischen Befunden oder klinischen Symptomen werden weiterführende Untersuchungen empfohlen [3]. Ergibt sich kein Verdacht auf eine Neuropathie, sollte das Screening einmal jährlich wiederholt werden.
Differenzialdiagnosen
Die diabetische Neuropathie ist eine Ausschlussdiagnose, da es sich um eine Schädigung der peripheren Nerven handelt, die infolge eines Diabetes mellitus ohne andere Ursachen auftritt [3]. Aber: Nicht jede Neuropathie bei Diabetespatient:innen ist zwingend eine diabetische Neuropathie. Die wichtigsten Differenzialdiagnosen aus Sicht der Allgemeinmediziner:in sind laut Expertenkonsens Neuropathien aufgrund von Alkoholabusus, Urämie, Hypothyreose, Paraproteinämie, monoklonale Gammopathie, neurotoxische Medikation, Vitamin-B12-Mangel, periphere arterielle Erkrankung, Krebs sowie entzündliche und infektiöse Erkrankungen [1].
Bei vielen Diabetiker:innen mit Nervenfunktionsstörungen liegt eine gemischte Pathogenese vor, z. B. die Kombination einer diabetischen Neuropathie- mit einer alkoholischen Neuropathie (Alkoholanamnese immer erheben!)
- mit einem Vitamin-B12-Mangel, vor allem unter Therapie mit Metformin oder Protonenpumpenhemmer (Vitamin-B12-Spiegel oder Holotranscobalamin bestimmen lassen) [8]
- mit einem Vitamin-B1-Mangel, der bei Diabetespatient:innen aufgrund der erhöhten Ausscheidung von Vitamin B1 im Urin ebenfalls häufig ist [9]. Ein Defizit fördert Nervenschäden und Störungen im Glukose-Metabolismus, die wiederum die Bildung gefäßschädigender Abbauprodukte wie AGEs forcieren [10].
In einer retrospektiven Studie bei 103 Diabetiker:innen mit DSPN wurden bei mehr als der Hälfte zusätzliche Neuropathie-Ursachen gefunden, am häufigsten Nieren- und chronische Darmerkrankungen [11].
Therapie ruht auf drei Säulen
Die wichtigsten Ziele der Therapie sind die Linderung der oft stark lebensqualitätsmindernden Symptome, die Zurückbildung der Nervenschäden bzw. zumindest das Aufhalten der Progression der Erkrankung sowie die Prävention eines diabetischen Fußsyndroms. Da die Pathomechanismen einer diabetischen Neuropathie komplex sind, ist eine multifaktorielle Therapie notwendig. Ist die Intervention nicht erfolgreich, schreitet eine DSPN fort. Zu den wichtigsten Risikofaktoren für eine DSPN zählen neben Diabetesdauer die Ausprägung der Hyperglykämie, arterielle Hypertonie und Hyperlipidämie [3]. Eine Hyperglykämie führt zu zellschädigenden Prozessen wie oxidativem Stress und Bildung aggressiver Advanced Glycation Endproducts (AGEs), die Folgeerkrankungen verursachen.
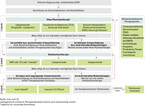
Im Konsensus zum Management der DSPN verweisen die Expert:innen auf einen holistischen Ansatz, basierend auf drei Grundsteinen:- Optimierung der Blutzuckerkontrolle, Lebensstilmodifikationen und Kontrolle von kardiovaskulären und anderen Risikofaktoren,
- pathogenetisch orientierte Pharmakotherapie und
- symptomatische Pharmakotherapie im Falle einer schmerzhaften DSPN [1] (Abb. 2).
1. Kausale Therapie
(optimale Diabetesbehandlung inklusive Lebensstilmodifikation und Behandlung kardiovaskulärer Risikofaktoren)
Es gibt großen Konsens, dass sowohl bei Typ-1- als auch Typ-2-Diabetiker:innen die Blutzuckerkontrolle optimiert werden sollte, um einer DSPN vorzubeugen bzw. die Progression einer bereits bestehenden DSPN zu verlangsamen [1]. Gute Evidenz dafür gibt es bisher aber nur bei Typ-1-Diabetiker:innen. In der DCCT-Studie wurde durch eine intensivierte Insulintherapie das Auftreten einer DSPN um 69 % (p=0,006) nach fünf Jahren im Vergleich zur Kontrollgruppe reduziert [15]. Die Progression der DSPN konnte um 57 % gebremst werden.
Bei Typ-2-Diabetiker:innen schützt eine intensivierte Diabetestherapie nach bisherigen Studien weniger eindeutig vor einer Neuropathie, umso wichtiger scheint eine multifaktorielle Lebensstilintervention zu sein. In der Look AHEAD-Studie konnte eine mehrjährige Lebensstilintervention bei Typ-2-Diabetiker:innen mit einer Reduktion neuropathischer Symptome assoziiert werden [16]. In einer weiteren Studie bei Personen mit gestörter Glukosetoleranz und Neuropathie konnte nach einjähriger Lebensstilintervention mittels Hautbiopsie eine Zunahme der Nervenfaserdichte nachgewiesen werden [17].
2. Pathogenetisch orientierte Pharmakotherapie
Ziel ist es, in die multifaktorielle Pathogenese der DSPN einzugreifen und pathogene Stoffwechselwege, die durch Hyperglykämien aktiviert werden – wie die Bildung reaktiver Sauerstoffradikale und AGEs, die Überaktivität der Proteinkinase C, den Polyol- und Hexosamin-Stoffwechselweg –, zu blockieren. Für die klinische Anwendung stehen in Deutschland das Antioxidans Alpha-Liponsäure (ALA) und das fettlösliche Benfotiamin, ein Vitamin-B1-Prodrug, zur Verfügung. Beide Substanzen konnten in klinischen Studien Symptome der DSPN verbessern und haben auch in der Langzeittherapie ein gutes Sicherheitsprofil.
Benfotiamin, das circa 5-fach höher bioverfügbar als herkömmliches Thiamin ist [21], kann den bei Diabetiker:innen häufigen Vitamin-B1-Mangel ausgleichen und so pathogene Stoffwechselwege hemmen. In einer sechs-wöchigen placebokontrollierten Studie bei 165 Patient:innen mit DSPN wurde mit hochdosiertem Benfotiamin (600 mg täglich) in der Per-Protokoll-Analyse der Neuropathie-Symptomen-Score signifikant verringert. Die Effekte waren bei hochdosierter Therapie ausgeprägter als bei einer niedrigeren Dosis (300 mg täglich) und nahmen mit zunehmender Studiendauer zu [22]. Ähnliche Ergebnisse wurden in einer weiteren placebokontrollierten Studie über drei Wochen bei insgesamt 40 Diabetiker:innen mit DSPN erzielt, die mit täglich 400 mg Benfotiamin behandelt wurden [23]. In einer weiteren Studie mit einer Behandlungszeit von bis zu zwölf Monaten (600 mg/Tag über drei Monate, gefolgt von 300 mg/Tag) wurde eine kontinuierliche Verringerung neuropathischer Symptome beobachtet [24].
Mit ALA, intravenös oder oral verabreicht, können sowohl neurologische Symptome als auch Defizite verbessert werden. Für eine i.v. Therapie über drei Wochen wurde dies in einer Metaanalyse mit insgesamt 1.258 Personen mit DSPN belegt [18], für die orale Therapie (600 mg, 1.200 mg oder 1.800 mg/Tag) in einer fünfwöchigen Studie [19]. In der Nathan-1-Studie, mit einer Dauer von vier Jahren die längste Studie bei DSPN, wurde unter oraler Therapie mit 600 mg ALA/Tag im Vergleich zu Placebo eine signifikante Reduktion von Defiziten nachgewiesen [20].
Die pathogenetisch orientierte Pharmakotherapie, zusätzlich zu Lebensstilinterventionen und Optimierung der Blutzuckereinstellung, wird bei Patient:innen mit asymptomatischer DSPN, mit symptomatischer nichtschmerzhafter DSPN und bei schmerzhafter DSPN empfohlen und sollte bei Patient:innen mit ausgeprägten neuropathischen Schmerzen durch eine symptomatische Behandlung ergänzt werden (Abb. 2) [1, 3, 25].
3. Symptomatische Schmerzbehandlung
In einzelnen Metaanalysen wurden Medikamente zur Behandlung neuropathischer Schmerzen – Antidepressiva, Antikonvulsiva, Opioide, Capsaicin-Pflaster – zum Teil unterschiedlich bewertet. Abhängig von der Intensität der Schmerzen und vom individuellen Risikoprofil der Patient:in sollte das am besten geeignete Medikament ausgewählt werden. Im Expertenkonsensus werden als Analgetika der ersten Wahl die Antikonvulsiva Gabapentin und Pregabalin und die Antidepressiva Duloxetin und Amitriptylin genannt (Abb. 3); als Medikamente der zweiten Wahl werden Tramadol und der dritten Wahl stärkere Opioide empfohlen [1]. Zusätzlich können topische Analgetika wie Capsaicin-Salbe oder -Pflaster (dritte Wahl) eingesetzt werden. Herkömmliche Analgetika wie NSAR sind für die Behandlung neuropathischer Schmerzen nicht geeignet.
Mit jeder Monotherapie wird laut klinischen Studien nur eine Ansprechrate von maximal 50 % erreicht. Deshalb ist häufig eine Kombination mehrerer Analgetika erforderlich, wobei sorgfältig auf das Risiko für Arzneimittelinteraktionen geachtet werden sollte. Eine ungenügende Wirksamkeit der Schmerztherapie sollte erst nach zwei- bis vierwöchiger Behandlungsdauer in adäquater Dosis festgestellt werden [1]. Auch nichtpharmakologische Optionen, wie psychologische Unterstützung, Physiotherapie, transkutane, elektrische Nervenstimulation und Akupunktur, sollten trotz der relativ geringen Evidenzlage in Betracht gezogen werden (Abb. 3), so die Empfehlung des Expertengremiums.
Mangel ausgleichen
Gedacht werden sollte bei Diabetiker:innen außerdem an häufige Mangelerscheinungen wie Vitamin-B12- oder Magnesiummangel, die ggf. ausgeglichen werden sollten. Es gibt Hinweise dafür, dass durch eine Vitamin-B12- bzw. Magnesiumsubstitution Symptome einer DSPN verringert werden können [1]. So zeigte sich in einer aktuellen placebokontrollierten klinischen Studie, dass bei Typ-2-Diabetes-Patient:innen mit DSPN und leicht erniedrigten Vitamin-B12-Spiegeln durch eine hochdosierte orale Vitamin-B12-Supplementation (1.000 g/d) die neurophysiologischen Parameter und der Schmerz-Score gegenüber der Kontrollgruppe signifikant gebessert werden konnten [26].
Prävention eines diabetischen Fußsyndroms
Patient:innen mit neurologischen Defiziten haben ein erhöhtes Risiko, ein diabetisches Fußsyndrom zu entwickeln. Zur Vorbeugung sollten die Patient:innen zu folgenden Maßnahmen angeleitet werden:- Tägliche Inspektion der Füße.
- Tragen von komfortablen, nicht zu engen Schuhen. Bei Bedarf sind die Patient:innen mit Diabetesschutzschuhen mit Weichpolstersohle, ggf. mit orthopädischer Schuhzurichtung, zu versorgen.
- Regelmäßige Fußpflege unter Vermeidung von spitzen und scharfen Gegenständen.
- Zeitnahe Vorstellung, sobald Wunden entstehen.
Bei allen Patient:innen mit diabetischer Neuropathie sollten, abhängig von der individuellen Krankheitssituation, zumindest halbjährliche Verlaufskontrollen erfolgen. Liegen zusätzlich eine pAVK und/oder Fußdeformitäten vor, werden alle drei Monate Kontrollen empfohlen [3]. Während der COVID-19-Pandemie gewinnen laut Expertenkonsensus auch telemedizinische Arzt-Patienten-Kontakte an Bedeutung, die z. B. für Verlaufskontrollen und die Beurteilung neuropathischer Beschwerden genutzt werden können [1].
Fazit
Eine diabetische Neuropathie ist bei Diabetiker:innen häufig und besteht oft bereits im Frühstadium der Erkrankung. Zur Früherkennung ist ein regelmäßiges Screening erforderlich, das allerdings in der Praxis noch nicht konsequent umgesetzt wird. Um ein Fortschreiten der Nervenschäden zu verhindern und die Symptomatik zu verringern, sollten alle Möglichkeiten der Intervention genutzt werden. Dazu zählen Optimierung der Blutzuckereinstellung, Anleitung zu einem gesunden Lebensstil, Blockade pathogener Stoffwechselwege mit Benfotiamin und/oder Alpha-Liponsäure, Vitamin-Substitution (z. B. Vitamin B12) und adäquate Therapie neuropathischer Schmerzen. Bei der Behandlung von Patient:innen mit diabetischer Neuropathie besteht derzeit eine Unterversorgung.
Dieser CME-Beitrag wird unterstützt von Wörwag Pharma
Auf unserem CME-Portal www.kirchheim-forum-cme.de können Sie ab dem 10.02.2022 diesen Beitrag bearbeiten und bekommen bei Erfolg Ihre Punkte sofort gutgeschrieben.