Asthma und COPD sind mit die häufigsten chronischen Atemwegserkrankungen in der Hausarztpraxis. Ihnen ist die unterschiedlich auftretende Luftnot gemein. Aber es gibt auch noch andere, seltene pneumologische Ursachen für Luftnot. Es gilt aufmerksam zu bleiben und nicht vorschnell eine dieser beiden Krankheiten anzunehmen.
Wir Hausärzt:innen haben gegenüber den anderen Fachrichtungen die Möglichkeit einer Frühdiagnose. Nur wir sehen die Frühzeichen. Damit tragen wir aber auch eine große Verantwortung. Sieht die Patient:in eine Fachkolleg:in, ist in der Regel einige Zeit verstrichen und die Krankheit hat viel Zeit gehabt, ungehindert fortschreiten zu können.
Ein Beispiel aus der Praxis
Herr K., 34 Jahre alt, macht aktuell eine Suchttherapie (Amphetamin, Cannabis). Er stellt sich in der Praxis vor, weil er bei Spaziergängen wegen Luftnot immer der Letzte ist, der nach leichten Anstiegen oben ankommt. Anfälle von Luftnot können nicht erfragt werden.
Es sind zahlreiche Allergien bekannt, die er aber nicht konkretisieren kann. Er raucht etwa 10 Zigaretten / Tag. Vor 5 Jahren ist von seinem damaligen Hausarzt ein Asthma diagnostiziert worden. Seitdem inhaliert er fast regelmäßig die Fixkombination ICS + LABA (Fluticason 250 + Salmeterol 50) 2 x/Tag, verspürt allerdings keine Linderung. Auskultatorisch deutlich abgeschwächtes Atemgeräusch ohne Nebengeräusche.
Ist das wirklich Asthma?
Bereits das Fehlen von anfallsartiger Luftnot, sondern ausschließlich (?) bei Belastung, und auch das fehlende Ansprechen der antientzündlichen Therapie, aber auch das abgeschwächte Atemgeräusch sprechen eher gegen ein Asthma und sollten aufhorchen lassen!
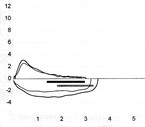
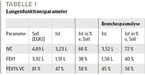
Die Lungenfunktion belegt Hinweise auf eine leichte Obstruktion. Bedeutsamer sind allerdings die deutlich reduzierte Vitalkapazität (IVC), der reduzierte Tiffeneau-Index (FEV1%VC) und die Einsekundenkapazität (FEV1) mit nahezu ausbleibender Änderung im akuten Bronchospasmolysetest (vgl. Tabelle 1/Abb. 1). Es stellt sich die Frage, wie die Diagnose Asthma gestellt werden konnte. Es steht zu befürchten, dass der Kollege vor 5 Jahren entweder keine Lungenfunktion gemacht oder einen Bronchospasmolysetest unterlassen hat.
Merke: Die Änderung oder ausbleibende Änderung der FEV1 (>15 %) im akuten Bronchospasmolysetest ist das wichtigste, einfache Unterscheidungsmerkmal zwischen Asthma und COPD! Bei einer Exazerbation mit Schleimhautschwellung verschwindet diese Reaktion zunehmend.
Die wichtigen Lungenfunktionsparameter (Tabelle 1) sind alle deutlich erniedrigt, was eigentlich gegen ein Asthma spricht. Die fehlende Änderung im akuten Bronchospasmolysetest erhärtet diese Feststellung. Eine ausbleibende Änderung würden wir beim Asthma nur sehen, wenn nur eine geringe oder keine Obstruktion vorliegt, also der Patient gut therapiert ist.
Die Laboranalyse zeigt: BSG 4/10, Erythrozyten 5,1 Mio./µl, Leukozyten 6,6, Tsd./µl, normale Verteilung, Eosinophile 6%, Normalwerte für Leber und Nierenwerte, Kalzium, Eisen, Kalium, Alpha-1-Antitrypsin 122 mg/dl (normal 88–174). Die Raucheranamnese und der Typ der Luftnot (Belastungsdyspnoe) könnten als Hinweis auf eine COPD gewertet werden, doch spricht das noch junge Alter gegen diese Diagnose. Ein Alpha-1-Antitrypsinmangel als Auslöser für den großen Lungenfunktionsverlust konnte ausgeschlossen werden.
Merke: Bei schnell fortschreitendem Lungenfunktionsverlust immer einen Alpha-1-Antitrypsin-Mangel mittels Laboruntersuchung ausschließen!
Ein zur Sicherheit vorgenommener verzögerter Bronchospasmolysetest (5 Tage 30 mg Prednisolon) zum Ausschluss einer "fixierten" Obstruktion blieb erwartungsgemäß ebenfalls negativ.
Alle Hinweise deuten auf eine restriktive Lungenerkrankung mit leichter obstruktiver Komponente ohne Änderung im Broncholysetest hin, also vermutlich nicht asthmatischer Genese.
Merke: Restriktive Ventilationsstörung = niedrige VC (wegen der Kompression bei forcierter Exspiration immer als IVC gemessen) bei normaler oder hochnormaler FEV1.
Röntgen-Thorax
Verdacht auf interstitielle Lungengerüsterkrankung, z. B. Fibrose.
Berufsanamnese
Während seiner beruflichen Tätigkeit war Herr K. auch für ein Jahr in einem Galvanisierbetrieb Salpetersäure ausgesetzt. Der Fall wurde zur Sicherheit der zuständigen Berufsgenossenschaft angezeigt. (Das Gesetz verpflichtet uns, bereits den Verdacht auf eine Berufserkrankung der Berufsgenossenschaft mitzuteilen.)
HF CT : Zeichen einer Drug Induced Fibrose
Die daraufhin erneut vorgenommene gezielte Anamnese konnte die wahrscheinliche Ursache der Fibrose klären. Herr K. hatte die Amphetamine über 15 Jahre pulverisiert und zur Effektsteigerung inhaliert. Im vorliegenden Fall hat die fortgesetzte Inhalation von Talkum zu einer Talkose mit Übergang in eine Fibrose geführt. Die Diagnose lautet hier also:Pneumokoniose, hier Talkose mit Übergang in eine Fibrose.
Pneumokoniosen (griech. Staublunge)
Unter Pneumokoniosen sind Lungenkrankheiten zusammengefasst, die nach Inhalation von vorwiegend anorganischen Stäuben auftreten. Im Röntgenbild sieht man fleckförmige interstitielle oder subpleurale Infiltrate oder auch kleine Zysten.
Um symptomatischen Patient:innen möglichst schnell eine antifibrotische Therapie zukommen zu lassen, sollte die Verdachtsdiagnose möglichst umgehend mittels standardisierter Anamneseerhebung, serologischer Testung und zellulärer Analyse der bronchoalveolären Lavage und hochauflösender Computertomografie in Dünnschnitttechnik gesichert werden [1].
Bei zeitlich begrenzter Inhalation besteht die Chance einer Spontanheilung. Bei fortgesetzter Exposition entwickelt sich eine chronische Erkrankung mit unterschiedlicher Prognose.
Eine eher schlechte Prognose mit einem möglichen Übergang in eine Lungenfibrose haben: Silikose (Quarzfeinstaub), Asbestfasern (Asbestose), Talkum (Talkose), Aluminiumstaub (Aluminose), Beryllium (Berylliose), Hartmetallstaub (Chrom, Titan, Vanadium, Wolfram und Molybdän).
Eine "eher" gute Prognose mit seltenem Übergang in eine Fibrose besitzen Anthrakose (Kohlestaub), Lungensiderose (Eisenstaub) und Barytose (Schwerspatstaub).
Pulmonale Fibrose (IPF)
Die Lungenfibrose kann idiopathisch sein oder als Folge einer Pneumokoniose auftreten [2]. Die Lungenfibrose (vgl. Tabelle 2) ist eine chronisch progrediente und letztlich tödlich verlaufende Krankheit, wobei, wie der Name bereits ausdrückt, die Ursache häufig unbekannt ist. Sie kann auch Folge einer Pneumokoniose sein (s. o.).
Wir haben nur eine Chance, die Progression durch antifibrotisch wirkende Substanzen zu reduzieren. Mit Hilfe dieser Therapie kann die Überlebenszeit bis zu 4–5 Jahre verlängert werden und die Patient:in kann vielleicht in den Genuss einer Lungentransplantation kommen. Voraussetzung ist allerdings eine möglichst frühzeitige Diagnose mit sofortigem Stopp einer eventuellen Exposition und frühzeitig begonnener und dauerhaft durchgeführter Therapie. Inhalatives Rauchen scheint sich negativ auf das Krankheitsbild auszuwirken.
Wann an Lungenfibrose denken?
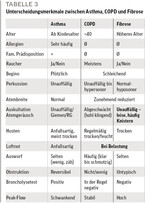
Wir wissen, dass sowohl ein Asthma als auch noch häufiger eine COPD lange Zeit nicht erkannt wird [3]. Für selten auftretende Krankheiten, wie z. B. Alpha-1-Antitrypsin-Mangel (24/100.000 Einwohner) und Fibrose (14–43/100.000), muss diese Feststellung demnach noch mehr gelten. Zu schnell werden diese seltenen Krankheitsbilder als Asthma oder COPD fehlgedeutet und damit falsch therapiert (vgl. Tabelle 3).
Die Kombination von Belastungsluftnot, trockenem Husten und einem Knistern bei der Auskultation (Sklerophonie bei 80–95 % der Patienten), das an das Lösen eines Klettverschlusses erinnert, sollte aufhorchen und an eine Lungenfibrose denken lassen.
Es gibt kein pneumologisches Krankheitsbild außer der Fibrose, wo dieses Phänomen zu auskultieren ist, und es tritt oftmals lange vor den typischen Veränderungen im Röntgenbild oder CT auf. Die Sklerophonie ist damit schon fast beweisend für eine Fibrose.
Sofern dieses Knistern auszukultieren ist, sollte man den Patienten ein paar Mal husten lassen und die Auskultation wiederholen. Ist die Sklerophonie weiter zu hören, ist das beweisend. Gelegentliche Symptome wie Müdigkeit, Schwächegefühl und Gewichtsverlust sind unspezifisch und ebenso wie Trommelschlegelfinger (20–30 %) im Spätstadium nicht wegweisend.
Merke: Bei Belastungsluftnot, Knistern bei der Auskultation und restriktiver Ventilationsstörung unbedingt Fibrose ausschließen!
Zu späte Diagnose kann fatale Folgen haben
Vom Beginn der Symptome bis zur Diagnose vergehen laut Literatur 1–2 Jahre, im geschilderten Fall waren es 5 (!) Jahre. In 50 % der Fälle wird eine falsche Diagnose gestellt, was bei einer medianen Überlebenszeit von 3–4 Jahren fatale Folgen hat.
Der Nachweis einer restriktiven Ventilationsstörung und die entsprechenden Hinweise im Röntgen-Thorax und CT sichern die Diagnose. Eine bronchoalveoläre Lavage (BAL) und in selteneren Fällen auch eine Lungenbiopsie können in der Differenzialdiagnose weiterhelfen.
Der Verlust an forcierter Vitalkapazität kann bis zu 200–280 ml/anno betragen, reduziert sich aber nicht linear, sodass die Prognose damit nicht vorhergesagt werden kann.
Da die meisten Patient:innen mit IPF Raucher sind, können COPD und Lungenemphysem gleichzeitig vorliegen. Weitere Komorbiditäten sind Bronchialkarzinom – häufiger als in der Normalbevölkerung –, kardiovaskuläre und thrombotische Erkrankungen, gastroösophagealer Reflux, Depression, schlafbezogene Atmungsstörungen und Diabetes.
Die Lungenfibrose zählt zu den seltenen Lungenerkrankungen und wird deswegen auch lange Zeit übersehen und dann eben auch häufig falsch therapiert. Bei der schlechten Prognose ist jeder Tag bis zum Beginn einer Therapie lebensentscheidend. Die letztendlich notwendige Lungentransplantation kann bei korrekter Therapie um eine gewisse Zeit hinausgezögert werden!
- Die Änderung oder ausbleibende Änderung der FEV1 (>15 %) im akuten Bronchospasmolysetest ist das wichtigste, einfache Unterscheidungsmerkmal zwischen Asthma und COPD.
- Die Kombination von Belastungsluftnot, trockenem Husten und einem Knistern bei der Auskultation sollte aufhorchen und an eine Lungenfibrose denken lassen.
Dr. med. Thomas Hausen
Erschienen in: doctors|today, 2022; 2 (6) Seite 45-48